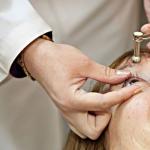
Лекция для врачей "Ургентные (неотложные) ситуации при детской эхокардиографии, верный диагноз – это жизнь". Проводит лекцию ФГБУ НИИ кардиологии ОО РАМН, Томск, А.А Сколов.
ВРОЖДЁННЫЕ ПОРОКИ СЕРДЦА
Врождённые пороки сердца обнаруживают у 1% рождённых живыми детей. Большинство этих больных погибают в младенческом и детском возрасте, и только 5-15% доживают до пубертатного периода. При своевременной хирургической коррекции врождённого порока сердца в детском возрасте продолжительность жизни больных значительно больше. Без хирургической коррекции обычно доживают до взрослого возраста пациенты с небольшими ДМЖП (дефект межжелудочковой перегородки), небольшими ДМПП (дефект межпредсердной перегородки), умеренным стенозом лёгочной артерии, открытым артериальным протоком небольших размеров, двустворчатым аортальным клапаном, незначительным стенозом устья аорты, аномалией Эбштайна, корригированной транспозицией магистральных сосудов. Реже доживают до взрослого периода больные с тетрадой Фалло и открытым АВ-каналом.
ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
ДМЖП (дефект межжелудочковой перегородки) - наличие сообщения между левым и правым желудочками, приводящее к патологическому сбросу крови из одной камеры сердца в другую. Дефекты могут располагаться в мембранозной (верхней) части межжелудочковой перегородки (75-80% всех дефектов), в мышечной части (10%), в выносящем тракте правого желудочка (надгребневые - 5%), в приносящем тракте (дефекты предсердно-желудочковой перегородки - 15%). Для дефектов, расположенных в мышечной части межжелудочковой перегородки, используют термин "болезнь Толочинова-Роже".
Распространённость
ДМЖП (дефект межжелудочковой перегородки) - наиболее частый врождённый порок сердца у детей и подростков; у взрослых он встречается менее часто. Это связано с тем, что в детском возрасте пациенты подвергаются оперативному вмешательству, у части детей ДМЖП (дефект межжелудочковой перегородки) закрываются самостоятельно (возможность самостоятельного закрытия сохраняется даже в зрелом возрасте при малых дефектах), а значительная часть детей с большими дефектами погибает. У взрослых обычно выявляют дефекты малого и среднего размера. ДМЖП (дефект межжелудочковой перегородки) может сочетаться с другими врождёнными пороками сердца (в порядке убывания частоты): коарктация аорты, ДМПП (дефект межпредсердной перегородки), открытый артериальный проток, подклапанный стеноз лёгочной артерии, подклапанный стеноз устья аорты, стеноз митрального отверстия.
ГЕМОДИНАМИКА
У взрослых ДМЖП (дефект межжелудочковой перегородки) сохраняются в связи с тем, что они либо не были выявлены в детском возрасте, либо не были своевременно прооперированы (рис. 9-1). Патологические изменения при ДМЖП (дефект межжелудочковой перегородки) зависят от размеров отверстия и сопротивления лёгочных сосудов.
Рис. 9-1. Анатомия и гемодинамика при ДМЖП (дефект межжелудочковой перегородки). А - аорта; ЛА - лёгочная артерия; ЛП - левое предсердие; ЛЖ - левый желудочек; ПП - правое предсердие; ПЖ - правый желудочек; НПВ - нижняя полая вена; ВПВ - верхняя полая вена. Короткой сплошной стрелкой указан дефект межжелудочковой перегородки.При ДМЖП (дефект межжелудочковой перегородки) малого размера (менее 4-5 мм), так называемом рестриктивном дефекте, сопротивление кровотоку через шунт высокое. Лёгочный кровоток увеличивается незначительно, давление в правом желудочке и сопротивление лёгочных сосудов нарастают также незначительно.
При ДМЖП (дефект межжелудочковой перегородки) средних размеров (5-20 мм) возникает умеренное увеличение давления в правом желудочке, обычно не превышающее половины давления в левом желудочке.
При большом ДМЖП (более 20 мм, нерестриктивный дефект) нет никакого сопротивления кровотоку, и уровни давлений в правом и левом желудочках равны. Увеличение объёма крови в правом желудочке приводит к усилению лёгочного кровотока и увеличению лёгочного сосудистого сопротивления. При значительном увеличении лёгочного сосудистого сопротивления сброс крови слева направо через дефект уменьшается, и при преобладании лёгочного сосудистого сопротивления над сопротивлением в большом круге кровообращения может возникать сброс крови справа налево с появлением цианоза. При большом сбросе крови слева направо развивается лёгочная гипертензия и необратимый склероз лёгочных артериол (синдром Айзенменгера).
У некоторых больных перимембранозные ДМЖП (дефект межжелудочковой перегородки) или дефекты в области выносящего тракта правого желудочка могут сочетаться с аортальной регургитацией в результате провисания створки аортального клапана в дефект.
Жалобы
Малые по размеру (рестриктивные) дефекты протекают бессимптомно. ДМЖП (дефект межжелудочковой перегородки) средних размеров приводят к отставанию в физическом развитии и частым инфекциям дыхательных путей. При больших дефектах, как правило, у больных имеются признаки право- и левожелудочковой недостаточности: одышка при физической нагрузке, увеличение печени, отёки ног, ортопноэ. При возникновении синдрома Айзенменгера больных начинают беспокоить выраженная одышка даже при незначительной физической нагрузке, боли в грудной клетке без чёткой связи с физической нагрузкой, кровохарканье, эпизоды потери сознания.
Осмотр
Дети при ДМЖП (дефект межжелудочковой перегородки) средних размеров обычно отстают в физическом развитии, у них может обнаруживаться сердечный горб. Сброс крови справа налево приводит к появлению изменений пальцев рук в виде "барабанных палочек", цианозу, усиливающемуся при физической нагрузке, внешним признакам эритроцитоза (см. главу 55 "Опухоли системы крови" раздел 55.2 "Хронические лейкозы").
Пальпация
Обнаруживают систолическое дрожание в средней части грудины, связанное с турбулентным током крови через ДМЖП (дефект межжелудочковой перегородки).
Аускультация сердца
Наиболее характерный признак - грубый систолический шум вдоль левого края грудины с максимумом в III-IV межреберьях слева с иррадиацией в правую половину грудной клетки. Между громкостью систолического шума и размером ДМЖП (дефект межжелудочковой перегородки) чёткой корреляции нет - тонкая струя крови через маленький ДМЖП может сопровождаться громким шумом (справедливо высказывание "много шума из ничего"). ДМЖП больших размеров может вообще не сопровождаться шумом из-за уравнивания давления крови в левом и правом желудочках. Кроме шума, при аускультации нередко выявляют расщепление II тона в результате удлинения систолы правого желудочка. При наличии надгребневого ДМЖП (дефект межжелудочковой перегородки) обнаруживают диастолический шум сопутствующей недостаточности аортального клапана. Исчезновение шума при ДМЖП - признак не улучшения, а ухудшения состояния, появляющийся в результате уравнивания давления в левом и правом желудочках.
Электрокардиография
ЭКГ при малых дефектах не изменена. При ДМЖП (дефект межжелудочковой перегородки) среднего размера имеются признаки гипертрофии левого предсердия и левого желудочка, отклонение электрической оси сердца влево. При ДМЖП (дефект межжелудочковой перегородки) больших размеров на ЭКГ возможно появление признаков гипертрофии левого предсердия и обоих желудочков.
Рентгенологическое исследование
При небольших дефектах изменений не обнаруживают. При значительном сбросе крови слева направо выявляют признаки увеличения правого желудочка, усиление сосудистого рисунка из-за нарастания лёгочного кровотока и лёгочной гипертензии. При лёгочной гипертензии наблюдаются её характерные рентгенологические признаки.
Эхокардиография
В двухмерном режиме можно непосредственно визуализировать ДМЖП (дефект межжелудочковой перегородки) . С помощью допплеровского режима обнаруживают турбулентный поток крови из одного желудочка в другой, оценивают направление сброса (слева направо или справа налево), а также определяют давление в правом желудочке по градиенту давления между желудочками.
Катетеризация полостей сердца
Катетеризация полостей сердца позволяет выявить высокое давление в лёгочной артерии, величина которого имеет решающее значение для определения тактики ведения больного (оперативное или консервативное). При катетеризации можно определить соотношение лёгочного кровотока и кровотока в большом круге кровообращения (в норме соотношение менее 1,5:1).
ЛЕЧЕНИЕ
ДМЖП (дефект межжелудочковой перегородки) малых размеров обычно не требуют хирургического лечения в связи с благоприятным течением. Хирургическое лечение ДМЖП (дефект межжелудочковой перегородки) не проводят также при нормальном давлении в лёгочной артерии (отношение лёгочного кровотока к кровотоку в большом круге кровообращения менее чем 1,5-2:1). Оперативное лечение (закрытие ДМЖП) показано при среднем или большом ДМЖП (дефект межжелудочковой перегородки) с отношением лёгочного кровотока к системному более 1,5:1 или 2:1 при отсутствии высокой лёгочной гипертензии. Если сопротивление лёгочных сосудов составляет 1/3 и менее от сопротивления в большом круге кровообращения, то прогрессирования лёгочной гипертензии после операции обычно не наблюдается. При наличии до операции среднего или выраженного повышения сопротивления лёгочных сосудов после радикальной коррекции порока лёгочная гипертензия сохраняется (она может даже прогрессировать). При больших дефектах и увеличении давления в лёгочной артерии результат хирургического лечения непредсказуем, так как, несмотря на закрытие дефекта, сохраняются изменения в сосудах лёгких.
Необходимо проводить профилактику инфекционного эндокардита (см. главу 6 "Инфекционный эндокардит").
ПРОГНОЗ
Прогноз обычно благоприятный при своевременно проведённом оперативном лечении. Риск инфекционного эндокардита при ДМЖП (дефект межжелудочковой перегородки) составляет 4%, что требует своевременной профилактики этого осложнения.
ТЕТРАДА ФАЛЛО
Тетрада Фалло - врождённый порок сердца, характеризующийся наличием четырёх компонентов: 1) большого высокорасположенного ДМЖП (дефект межжелудочковой перегородки); 2) стеноза лёгочной артерии; 3) декстропозиции аорты; 4) компенсаторной гипертрофии правого желудочка.
Распространённость
Тетрада Фалло составляет 12-14% всех врождённых пороков сердца.
ГЕМОДИНАМИКА
При тетраде Фалло аорта располагается над большим ДМЖП (дефект межжелудочковой перегородки) и над обоими желудочками, в связи с чем систолическое давление в правом и левом желудочках одинаковое (рис. 9-2). Главный гемодинамический фактор - отношение между сопротивлением кровотоку в аорте и в стенозированной лёгочной артерии.

При небольшом сопротивлении в лёгочных сосудах лёгочный кровоток может быть вдвое больше кровотока в большом круге кровообращения, и насыщение артериальной крови кислородом может быть нормальным (ацианотичная тетрада Фалло).
При значительном сопротивлении лёгочному кровотоку возникает сброс крови справа налево, в результате чего возникают цианоз и полицитемия.
Стеноз лёгочной артерии может быть инфундибулярным или комбинированным, реже клапанным (подробнее об этом см. в главе 8 "Приобретённые пороки сердца").
При физической нагрузке происходит увеличение притока крови к сердцу, но кровоток через малый круг кровообращения не возрастает из-за стенозированной лёгочной артерии, и избыточное количество крови сбрасывается в аорту через ДМЖП (дефект межжелудочковой перегородки), поэтому цианоз усиливается. Возникает гипертрофия, что приводит к усилению цианоза. Гипертрофия правого желудочка развивается вследствие постоянного преодоления препятствия в виде стеноза лёгочной артерии. В результате гипоксии развивается компенсаторная полицитемия - увеличивается количество эритроцитов и гемоглобина. Развиваются анастомозы между бронхиальными артериями и ветвями лёгочной артерии. У 25% больных обнаруживают правостороннее расположение дуги аорты и нисходящей аорты.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Основной жалобой взрослых больных тетрадой Фалло является одышка. Кроме того, могут беспокоить боли в сердце без связи с физической нагрузкой, сердцебиение. Больные склонны к лёгочным инфекциям (бронхиты и пневмонии).
Осмотр
Отмечают цианоз, степень выраженности которого может быть различной. Иногда цианоз настолько выражен, что синеют не только кожные покровы и губы, но также слизистая оболочка полости рта, конъюнктива. Характерно отставание в физическом развитии, изменение пальцев ("барабанные палочки"), ногтей ("часовые стёкла").
Пальпация
Обнаруживают систолическое дрожание во II межреберье слева от грудины над участком стеноза лёгочной артерии.
Аускультация сердца
Выслушивают грубый систолический шум стеноза лёгочной артерии во II-III межреберьях слева от грудины. II тон над лёгочной артерией ослаблен.
Лабораторные исследования
Общий анализ крови: высокий эритроцитоз, повышение содержания гемоглобина, СОЭ резко снижена (до 0-2 мм/ч).
Электрокардиография
Электрическая ось сердца обычно смещена вправо (угол α от +90° до +210°), отмечают признаки гипертрофии правого желудочка.
Эхокардиография
ЭхоКГ позволяет обнаружить анатомические составляющие тетрады Фалло.
Рентгенологическое исследование
Отмечают повышенную прозрачность лёгочных полей из-за уменьшения кровенаполнения лёгких. Контуры сердца имеют специфическую форму "деревянного башмака сабо": уменьшенная дуга лёгочной артерии, подчёркнутая "талия сердца", закруглённая и приподнятая над диафрагмой верхушка сердца. Дуга аорты может быть справа.
ОСЛОЖНЕНИЯ
Наиболее часто возникают инсульты, ТЭЛА, выраженная сердечная недостаточность, инфекционный эндокардит, абсцессы мозга, разнообразные аритмии.
ЛЕЧЕНИЕ
Единственный метод лечения - хирургический (радикальная операция - пластика дефекта, устранение стеноза лёгочной артерии и смещение аорты). Иногда хирургическое лечение состоит из двух этапов (первым этапом ликвидируют стеноз лёгочной артерии, а вторым проводят пластику ДМЖП (дефект межжелудочковой перегородки)).
ПРОГНОЗ
При отсутствии оперативного лечения до 40-летнего возраста доживают 3% больных с тетрадой Фалло. Летальные исходы наступают из-за инсультов, абсцессов мозга, выраженной сердечной недостаточности, инфекционного эндокардита, аритмий.
ПЕНТАДА ФАЛЛО
Пентада Фалло - врождённый порок сердца, состоящий из пяти компонентов: четырёх признаков тетрады Фалло и ДМПП (дефект межпредсердной перегородки). Гемодинамика, клиническая картина, диагностика и лечение аналогичны таковым при тетраде Фалло и ДМПП (дефект межпредсердной перегородки).
ДЕФЕКТ МЕЖПРЕДСЕРДНОЙ ПЕРЕГОРОДКИ
ДМПП (дефект межпредсердной перегородки) - наличие сообщения между левым и правым предсердиями, приводящее к патологическому сбросу крови (шунтированию) из одной камеры сердца в другую.
Классификация
По анатомической локализации различают первичный и вторичный ДМПП (дефект межпредсердной перегородки), а также дефект венозного синуса.
Первичный ДМПП (дефект межпредсердной перегородки) располагается ниже овальной ямки и является составной частью врождённого порока сердца, называемого открытым предсердно-желудочковым каналом.
Вторичный ДМПП (дефект межпредсердной перегородки) располагается в области овальной ямки.
Дефект венозного синуса представляет собой сообщение верхней полой вены с обоими предсердиями, располагающееся над нормальной межпредсердной перегородкой.
Выделяют также ДМПП (дефект межпредсердной перегородки) других локализаций (например, венечного синуса), но они встречаются крайне редко.
Распространённость
ДМПП (дефект межпредсердной перегородки) составляет около 30% всех врождённых пороков сердца. Чаще его обнаруживают у женщин. 75% ДМПП (дефект межпредсердной перегородки) являются вторичными, 20% - первичными, 5% - дефектами венозного синуса. Данный порок часто сочетается с другими - стенозом лёгочной артерии, аномальным дренажом лёгочных вен, пролапсом митрального клапана. ДМПП (дефект межпредсердной перегородки) могут быть множественными.
ГЕМОДИНАМИКА
Сброс крови слева направо приводит к диастолической перегрузке правого желудочка и увеличению кровотока в лёгочной артерии (рис. 9-3). Направление и объём сбрасываемой через дефект крови зависят от размера дефекта, градиента давления между предсердиями и податливости (растяжимости) желудочков.

При рестриктивном ДМПП (дефект межпредсердной перегородки), когда площадь дефекта меньше площади предсердно-желудочкового отверстия, имеется градиент давления между предсердиями и сброс крови слева направо.
При нерестриктивном ДМПП (больших размеров) градиент давления между предсердиями отсутствует и объём шунтируемой через дефект крови регулируется податливостью (растяжимостью) желудочков. Правый желудочек более податлив (поэтому давление в правом предсердии падает быстрее, чем в левом), и сброс крови происходит слева направо, возникает дилатация правых отделов сердца и увеличивается кровоток через лёгочную артерию.
В отличие от ДМЖП (дефект межжелудочковой перегородки) давление в лёгочной артерии и лёгочное сосудистое сопротивление при ДМПП (дефект межпредсердной перегородки) долгое время остаются невысокими в связи с низким градиентом давления между предсердиями. Это объясняет тот факт, что ДМПП (дефект межпредсердной перегородки) в детском возрасте обычно остаётся нераспознанным. Клиническая картина ДМПП (дефект межпредсердной перегородки) проявляется с возрастом (старше 15-20 лет) в результате нарастания давления в лёгочной артерии и появления других осложнений - нарушений ритма сердца, правожелудочковой недостаточности [в последнем случае риск ТЭЛА и артерий большого круга (парадоксальной эмболии) высок]. С возрастом при больших ДМПП (дефект межпредсердной перегородки) возможно появление АГ из-за увеличения периферического сосудистого сопротивления в результате анатомического изменения лёгочных сосудов, также постепенно сброс крови становится двунаправленным. Реже сброс крови может быть справа налево.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Жалобы у больных с ДМПП (дефект межпредсердной перегородки) длительное время отсутствуют. Анамнестически выявляют частые заболевания дыхательных путей - бронхиты, пневмонии. Может беспокоить одышка, возникающая первоначально при нагрузке, а затем в покое, быстрая утомляемость. После 30 лет заболевание прогрессирует: развиваются сердцебиение (наджелудочковые аритмии и фибрилляция предсердий), признаки лёгочной гипертензии (см. главу 14 "Лёгочная гипертензия") и сердечной недостаточности по правожелудочковому типу.
Осмотр
Осмотр позволяет определить некоторое отставание в физическом развитии. Появление цианоза и изменение концевых фаланг пальцев в виде "барабанных палочек" и ногтей в виде "часовых стёкол" свидетельствуют об изменении направления сброса крови справа налево.
Пальпация
Определяется пульсация лёгочной артерии (при наличии лёгочной гипертензии) во II межреберье слева от грудины.
Аускультация сердца
При малых размерах дефекта аускультативных изменений не обнаруживают, поэтому обычно ДМПП (дефект межпредсердной перегородки) диагностируют при появлении признаков лёгочной гипертензии.
I тон сердца не изменён. II тон расщеплён вследствие значительного отставания лёгочного компонента II тона в результате протекания большого объёма крови через правые отделы сердца (удлинение систолы правого желудочка). Это расщепление является фиксированным, т.е. не зависит от фаз дыхания.
Выслушивают систолический шум над лёгочной артерией в результате выброса правым желудочком увеличенного объёма крови. При первичном ДМПП (дефект межпредсердной перегородки) на верхушке сердца выслушивают также систолический шум относительной недостаточности митрального и трёхстворчатого клапана. Над трёхстворчатым клапаном может выслушиваться низкочастотный диастолический шум из-за увеличения кровотока через трёхстворчатый клапан.
С увеличением сопротивления лёгочных сосудов и уменьшением сброса крови слева направо аускультативная картина изменяется. Усиливаются систолический шум над лёгочной артерией и лёгочный компонент II тона, оба компонента II тона могут сливаться. Кроме того, появляется диастолический шум недостаточности клапана лёгочной артерии.
Электрокардиография
При вторичном ДМПП (дефект межпредсердной перегородки) отмечают комплексы rSR ’ в правых грудных отведениях (как проявление задержки активации заднебазальных отделов межжелудочковой перегородки и расширения выносящего тракта правого желудочка), отклонение электрической оси сердца вправо (при гипертрофии и дилатации правого желудочка). При дефекте венозного синуса наблюдают АВ-блокаду I степени, нижнепредсердный ритм. Характерны нарушения ритма сердца в виде наджелудочковых аритмий и фибрилляции предсердий.
Рентгенологическое исследование
Рентгенологическое исследование обнаруживает дилатацию правого предсердия и правого желудочка, дилатацию ствола лёгочной артерии и двух её ветвей, симптом "пляски корней лёгких" (усиление пульсации в результате усиленного лёгочного кровотока вследствие сброса крови).
Эхокардиография
ЭхоКГ (рис. 9-4) помогает обнаружить дилатацию правого желудочка, правого предсердия и парадоксальное движение межжелудочковой перегородки. При достаточном размере дефекта его можно обнаружить в двухмерном режиме, особенно чётко в субксифоидальной позиции (когда положение межпредсердной перегородки перпендикулярно ультразвуковому лучу). Наличие дефекта подтверждают допплеровским УЗИ, позволяющим идентифицировать турбулентный поток шунтируемой крови из левого предсердия в правое или, наоборот, через межпредсердную перегородку. Обнаруживают также признаки лёгочной гипертензии.

Рис. 9-4. ЭхоКГ при ДМПП (двухмерный режим, четырёхкамерная позиция). 1 - правый желудочек; 2 - левый желудочек; 3 - левое предсердие; 4 - дефект межпредсердной перегородки; 5 - правое предсердие.
Катетеризация полостей сердца
Катетеризация полостей сердца проводится для определения степени выраженности лёгочной гипертензии.
ЛЕЧЕНИЕ
При отсутствии выраженной лёгочной гипертензии проводят хирургическое лечение - пластику ДМПП (дефект межпредсердной перегородки). При наличии симптомов сердечной недостаточности необходима терапия сердечными гликозидами, диуретиками, ингибиторами АПФ (подробнее об этом см. в главе 11 "Сердечная недостаточность"). Больным с первичным ДМПП, дефектом венозного синуса рекомендована профилактика инфекционного эндокардита (см. главу 6 "Инфекционный эндокардит").
ПРОГНОЗ
При своевременном оперативном лечении прогноз благоприятный. У неоперированных больных летальные исходы до 20-летнего возраста редки, но после 40 лет смертность достигает 6% в год. Основными осложнениями ДМПП (дефект межпредсердной перегородки) являются фибрилляция предсердий, сердечная недостаточность, редко парадоксальная эмболия. Инфекционный эндокардит при вторичном ДМПП возникает весьма редко. В случаях малого размера ДМПП больные доживают до глубокой старости.
ОТКРЫТЫЙ АРТЕРИАЛЬНЫЙ ПРОТОК
Открытый артериальный проток - порок, характеризующийся незаращением сосуда между лёгочной артерией и аортой (боталлов проток) в течение 8 нед после рождения; проток функционирует во внутриутробном периоде, но его незаращение приводит к нарушениям гемодинамики.
Распространённость
Открытый артериальный проток наблюдают в общей популяции с частотой 0,3%. Он составляет 10-18% всех врождённых пороков сердца.
ГЕМОДИНАМИКА
Наиболее часто артериальный проток соединяет лёгочную артерию и нисходящую аорту ниже отхождения левой подключичной артерии, реже он соединяет лёгочную артерию и нисходящую аорту выше отхождения левой подключичной артерии (рис. 9-5). Через 2-3 дня (реже через 8 нед) после рождения проток закрывается. У недоношенных детей, при гипоксии плода, перенесённой фетальной краснухе (в I триместре беременности) проток остаётся открытым. Возникает сброс (шунтирование) крови из нисходящей аорты в ствол лёгочной артерии. Дальнейшие проявления порока зависят от диаметра и длины открытого артериального протока и сопротивления кровотоку в самом протоке.

Рис. 9-5. Анатомия и гемодинамика при открытом артериальном протоке. А - аорта; ЛА - лёгочная артерия; ЛП - левое предсердие; ЛЖ - левый желудочек; ПП - правое предсердие; ПЖ - правый желудочек; НПВ - нижняя полая вена; ВПВ - верхняя полая вена. Сплошная часть стрелки обозначает патологический поток крови из аорты в лёгочные артерии.
При малом размере протока и высоком сопротивлении шунта объём сбрасываемой крови незначителен. Поступление избыточного количества крови в лёгочную артерию, левое предсердие и левый желудочек также мало. Направление сброса крови в течение систолы и диастолы остается постоянным (непрерывным) - слева (из аорты) направо (в лёгочную артерию).
При большом диаметре протока в лёгочную артерию будет поступать значительное избыточное количество крови, приводя к повышению давления в ней (лёгочной гипертензии) и перегружая левое предсердие и левый желудочек объёмом (следствием этого являются дилатация и гипертрофия левого желудочка). Со временем развиваются необратимые изменения в лёгочных сосудах (синдром Айзенменгера) и сердечная недостаточность. В дальнейшем давление в аорте и лёгочной артерии уравнивается, а затем в лёгочной артерии становится выше, чем в аорте. Это приводит к изменению направления сброса крови - справа (из лёгочной артерии) налево (в аорту). Впоследствии возникает правожелудочковая недостаточность.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Проявления порока зависят от размеров открытого артериального протока. Открытый артериальный проток с небольшим сбросом крови может не манифестировать в детском возрасте и проявиться с возрастом быстрой утомляемостью и одышкой при физической нагрузке. При большом объёме сбрасываемой крови с детства имеются жалобы на одышку при физической нагрузке, признаки ортопноэ, сердечной астмы, боли в правом подреберье вследствие увеличения печени, отёки ног, цианоз ног (в результате сброса крови справа налево в нисходящую аорту), цианоз левой руки (при открытом артериальном протоке выше отхождения левой подключичной артерии).
При малом объёме сброса крови слева направо внешних признаков порока нет. При сбросе крови справа налево появляется цианоз ног, изменения пальцев ног в виде "барабанных палочек", изменения пальцев левой руки в виде "барабанных палочек".
Пальпация
При интенсивном сбросе крови слева направо определяется систолическое дрожание грудной клетки над лёгочной артерией и супрастернально (в яремной ямке).
Аускультация сердца
Типичное аускультативное проявление открытого артериального протока - непрерывный систоло-диастолический ("машинный") шум из-за постоянного однонаправленного кровотока из аорты в лёгочную артерию. Этот шум высокочастотный, усиливается ко II тону, лучше выслушивается под левой ключицей и иррадиирует в спину. Кроме того, может выслушиваться среднедиастолический шум на верхушке сердца из-за увеличенного кровотока через левое предсердно-желудочковое отверстие. Звучность II тона бывает трудно определить из-за громкого шума. При уравнивании давления в аорте и лёгочной артерии шум из непрерывного систоло-диастолического превращается в систолический, а затем исчезает полностью. В этой ситуации начинает отчётливо выявляться акцент II тона над лёгочной артерией (признак развития лёгочной гипертензии).
Электрокардиография
Если сброс крови небольшой, патологических изменений не обнаруживают. При перегрузке левых отделов сердца большим объёмом избыточной крови отмечают признаки гипертрофии левого предсердия и левого желудочка. На фоне выраженной лёгочной гипертензии на ЭКГ выявляют признаки гипертрофии и правого желудочка.
Эхокардиография
При значительных размерах открытого артериального протока наблюдают дилатацию левого предсердия и левого желудочка. Открытый артериальный проток больших размеров можно выявить в двухмерном режиме. В допплеровском режиме в лёгочной артерии определяется турбулентный систоло-диастолический поток вне зависимости от размеров протока.
Рентгенологическое исследование
Если шунт имеет небольшие размеры, рентгенографическая картина обычно не изменена. При выраженном сбросе крови выявляют увеличение левых отделов сердца, признаки лёгочной гипертензии (выбухание ствола лёгочной артерии).
ЛЕЧЕНИЕ
При появлении признаков сердечной недостаточности назначают сердечные гликозиды и диуретики (см. главу 11 "Сердечная недостаточность"). Рекомендуется профилактика инфекционного эндартериита до и в течение шести месяцев после хирургической коррекции порока (см. главу 6 "Инфекционный эндокардит").
Хирургическое лечение в виде лигирования открытого артериального протока или окклюзии его просвета необходимо проводить до развития необратимых изменений со стороны сосудов лёгких. После оперативного лечения признаки лёгочной гипертензии могут сохраняться или даже прогрессировать.
ОСЛОЖНЕНИЯ
При открытом артериальном протоке могут возникать осложнения: инфекционный эндартериит, ТЭЛА, аневризма протока, её расслаивание и разрыв, кальцификация протока, сердечная недостаточность. Инфекционный эндартериит обычно развивается в лёгочной артерии напротив открытого артериального протока в результате постоянной травматизации струёй крови стенки лёгочной артерии. Частота развития инфекционного эндартериита достигает 30%.
ПРОГНОЗ
Своевременная операция позволяет устранить патологический сброс крови из аорты в лёгочную артерию, хотя признаки лёгочной гипертензии могут сохраняться в течение всей жизни. Средняя продолжительность жизни без оперативного лечения составляет 39 лет.
Для диагностики коарктации аорты имеет значение правильное измерение АД на ногах. Для этого больного укладывают на живот, манжету накладывают на нижнюю треть бедра и проводят аускультацию в подколенной ямке методикой, аналогичной таковой при измерении давления на руках (с определением систолического и диастолического уровней). В норме давление на ногах на 20-30 мм рт.ст. выше, чем на руках. При коарктации аорты давление на ногах значительно снижено или не определяется. Диагностическим признаком коарктации аорты считают разницу систолического (или среднего) АД на руках и ногах более 10-20 мм рт.ст. Нередко отмечают примерно равное давление на руках и ногах, но после физической нагрузки (тредмил) определяется значительная разница. Разница систолического АД на левой и правой руках говорит о том, что место отхождения одной из подключичной артерий расположено выше или ниже обструкции.
Пальпация
Определяют отсутствие или значительное ослабление пульса на ногах. Можно обнаружить увеличенные пульсирующие коллатерали в межреберьях, в межлопаточном пространстве.
Аускультация сердца
Выявляют акцент II тона над аортой из-за высокого АД. Характерен систолический шум в точке Боткина-Эрба, а также под левой ключицей, в межлопаточном пространстве и на сосудах шеи. При развитых коллатералях выслушивают систолический шум над межрёберными артериями. При дальнейшем прогрессировании гемодинамических нарушений выслушивается непрерывный (систоло-диастолический) шум.
Электрокардиография
Обнаруживают признаки гипертрофии левого желудочка.
Эхокардиография
При супрастернальном исследовании аорты в двухмерном режиме имеются признаки её сужения. При допплеровском исследовании определяют турбулентный систолический поток ниже места сужения и вычисляют градиент давления между расширенной и суженной частями аорты, что нередко имеет важное значение при принятии решения об оперативном лечении.
Рентгенологическое исследование
При длительном существовании коллатералей обнаруживают узурацию нижних частей рёбер как следствие сдавления их расширенными и извитыми межрёберными артериями. Для уточнения диагноза проводят аортографию, точно выявляющую место и степень коарктации.
ЛЕЧЕНИЕ
Радикальным методом лечения коарктации аорты является хирургическое иссечение суженного участка. Медикаментозную терапию проводят в зависимости от клинических проявлений порока. При явлениях сердечной недостаточности назначают сердечные гликозиды, диуретики, ингибиторы АПФ (подробнее см. главу 11 "Сердечная недостаточность"). Может возникнуть необходимость в лечении АГ.
ПРОГНОЗ И ОСЛОЖНЕНИЯ
Без оперативного лечения к 50 годам умирают 75% больных. В результате высокого АД возможно развитие типичных осложнений: инсультов, почечной недостаточности. Нетипичным осложнением АГ является развитие неврологических расстройств (например, нижнего парапареза, нарушение мочеиспускания) из-за сдавления расширенными межрёберными артериями корешков спинного мозга. К редким осложнениям относят инфекционный эндоаортит, разрыв расширенной аорты.
ВРОЖДЁННЫЙ СТЕНОЗ УСТЬЯ АОРТЫ
Врождённый стеноз устья аорты - сужение выносящего тракта левого желудочка в области аортального клапана. В зависимости от уровня расположения обструкции стеноз может быть клапанным, подклапанным, надклапанным.
Распространённость
Врождённый стеноз устья аорты составляет 6% от всех врождённых пороков сердца. Наиболее часто отмечают клапанный стеноз (80%), реже подклапанный и надклапанный. У мужчин стеноз устья аорты наблюдают в 4 раза чаще, чем у женщин.
ГЕМОДИНАМИКА
Клапанный стеноз (см. рис. 9-7). Наиболее часто аортальный клапан двустворчатый, при этом отверстие расположено эксцентрично. Иногда клапан состоит из одной створки. Реже клапан состоит из трёх створок, сращённых между собой одной или двумя спайками.

При подклапанном стенозе отмечают три вида изменений: дискретную мембрану под аортальными створками, туннель, мышечное сужение (субаортальная гипертрофическая кардиомиопатия, см. главу 12 "Кардиомиопатии и миокардиты").
Надклапанный стеноз устья аорты может быть в виде мембраны или гипоплазии восходящей части аорты. Признаком гипоплазии восходящей аорты считают отношение диаметра дуги аорты к диаметру восходящей аорты менее 0,7. Нередко надклапанный стеноз устья аорты сочетается со стенозом ветвей лёгочной артерии.
Надклапанный стеноз устья аорты в сочетании с умственной отсталостью называется синдромом Уильямса.
Стеноз устья аорты часто сочетается с другими врождёнными пороками сердца - ДМЖП (дефект межжелудочковой перегородки), ДМПП (дефект межпредсердной перегородки), открытым артериальным протоком, коарктацией аорты.
В любом случае создаётся препятствие кровотоку и развиваются изменения, приведённые в главе 8 "Приобретённые пороки сердца". Со временем развивается кальцификация клапана. Характерно развитие постстенотического расширения аорты.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Большинство больных при незначительном стенозе жалоб не предъявляют. Появление жалоб свидетельствует о выраженном стенозе устья аорты. Возникают жалобы на одышку при физической нагрузке, быструю утомляемость (из-за сниженного сердечного выброса), обмороки (в результате гипоперфузии мозга), загрудинные боли при физической нагрузке (из-за гипоперфузии миокарда). Возможно возникновение внезапной сердечной смерти, но в большинстве случаев этому предшествуют жалобы или изменения на ЭКГ.
Осмотр , перкуссия
См. раздел "Стеноз устья аорты" в главе 8 "Приобретённые пороки сердца".
Пальпация
Определяют систолическое дрожание вдоль правого края верхней части грудины и над сонными артериями. При пиковом систолическом градиенте давления менее 30 мм рт.ст. (по данным ЭхоКГ) дрожание не выявляется. Низкое пульсовое давление (менее 20 мм рт.ст.) свидетельствует о значительной выраженности стеноза устья аорты. При клапанном стенозе обнаруживают малый медленный пульс.
Аускультация сердца
Характерно ослабление II тона или его полное исчезновение вследствие ослабления (исчезновения) аортального компонента. При надклапанном стенозе устья аорты II тон сохранён. При клапанном стенозе устья аорты выслушивают ранний систолический клик на верхушке сердца, отсутствующий при над- и подклапанных стенозах. Он исчезает при выраженном клапанном стенозе устья аорты.
Основной аускультативный признак стеноза устья аорты - грубый систолический шум с максимумом во II межреберье справа и иррадиацией в сонные артерии, иногда вдоль левого края грудины к верхушке сердца. При подклапанном стенозе устья аорты наблюдают отличия в аускультативных проявлениях: не выслушивается ранний систолический клик, отмечают ранний диастолический шум недостаточности аортального клапана (у 50% больных).
Электрокардиография
При клапанном стенозе выявляют признаки гипертрофии левого желудочка. При надклапанном стенозе устья аорты ЭКГ может быть не изменена. При подклапанном стенозе (в случае субаортальной гипертрофической кардиомиопатии) возможно обнаружение патологических зубцов Q (узкие и глубокие).
Эхокардиография
В двухмерном режиме определяют уровень и характер обструкции аортального отверстия (клапанный, подклапанный, надклапанный). В допплеровском режиме оценивают пиковый систолический градиент давления (максимальный градиент давления при открытии створок аортального клапана) и степень стеноза устья аорты.
При пиковом систолическом градиенте давления (при нормальном сердечном выбросе) более 65 мм рт.ст. или площади аортального отверстия менее 0,5 см 2 /м 2 (в норме площадь аортального отверстия 2 см 2 /м 2) стеноз устья аорты считают выраженным.
Пиковый систолический градиент давления 35-65 мм рт.ст. или площадь аортального отверстия 0,5-0,8 см 2 /м 2 рассматривают как стеноз устья аорты средней степени.
При пиковом систолическом градиенте давления менее 35 мм рт.ст. или площади аортального отверстия более 0,9 см 2 /м 2 стеноз устья аорты считают незначительным.
Эти показатели информативны только при сохранённой функции левого желудочка и отсутствии аортальной регургитации.
Рентгенологическое исследование
Выявляют постстенотическое расширение аорты. При подклапанном стенозе устья аорты постстенотического расширения аорты нет. Возможно обнаружение кальцификатов в проекции аортального клапана.
ЛЕЧЕНИЕ
При отсутствии кальцификации проводят вальвулотомию или иссечение дискретной мембраны. При выраженных фиброзных изменениях показано протезирование аортального клапана.
ПРОГНОЗ И ОСЛОЖНЕНИЯ
Стеноз устья аорты обычно прогрессирует вне зависимости от уровня обструкции (клапанный, надклапанный, подклапанный). Риск развития инфекционного эндокардита составляет 27 случаев на 10 000 пациентов со стенозом устья аорты в год. При градиенте давления более 50 мм рт.ст. риск инфекционного эндокардита увеличивается в 3 раза. При стенозе устья аорты возможна внезапная сердечная смерть, особенно при физических нагрузках. Риск внезапной сердечной смерти увеличивается с нарастанием градиента давления - он более высокий у больных со стенозом устья аорты при градиенте давления более 50 мм рт.ст.
СТЕНОЗ ЛЁГОЧНОЙ АРТЕРИИ
Стеноз лёгочной артерии - сужение выносящего тракта правого желудочка в области клапана лёгочной артерии.
Распространённость
Изолированный стеноз лёгочной артерии составляет 8-12% всех врождённых пороков сердца. В большинстве случаев это клапанный стеноз (третий наиболее частый врождённый порок сердца), но он может также быть комбинированным (в сочетании с подклапанным, надклапанным стенозами, другими врождёнными пороками сердца).
ГЕМОДИНАМИКА
Сужение может быть клапанным (80-90% случаев), подклапанным, надклапанным.
При клапанном стенозе клапан лёгочной артерии может быть одностворчатым, двустворчатым и трёхстворчатым. Характерно постстенотическое расширение ствола лёгочной артерии.
Изолированный подклапанный стеноз характеризуется инфундибулярным (воронкообразным) сужением выносящего тракта правого желудочка и аномальным мышечным пучком, препятствующим выбросу крови из правого желудочка (оба варианта обычно сочетаются с ДМЖП (дефект межжелудочковой перегородки)).
Изолированный надклапанный стеноз может быть в виде локализованного стеноза, полной или неполной мембраны, диффузной гипоплазии, множественных периферических стенозов лёгочной артерии.
При сужении лёгочного ствола возникает увеличение градиента давления между правым желудочком и лёгочной артерией. Из-за препятствия на пути тока крови возникает гипертрофия правого желудочка, а затем его недостаточность. Это приводит к повышению давления в правом предсердии, открытию овального отверстия и сбросу крови справа налево с развитием цианоза и правожелудочковой недостаточности. У 25% больных стеноз лёгочной артерии сочетается со вторичным ДМПП (дефект межпредсердной перегородки).
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Незначительно выраженный стеноз лёгочной артерии в большинстве случаев протекает бессимптомно. При выраженном стенозе появляется быстрая утомляемость, одышка и боль в грудной клетке при физической нагрузке, цианоз, головокружение и обмороки. Одышка при стенозе лёгочной артерии возникает в результате неадекватной перфузии работающих периферических мышц, вызывающей рефлекторную вентиляцию лёгких. Цианоз при стенозе лёгочной артерии может быть как периферического (результат низкого сердечного выброса), так и центрального (результат сброса крови через открытое овальное отверстие) происхождения.
Осмотр
Можно обнаружить пульсацию увеличенного правого желудочка в надчревной области. При присоединении недостаточности трёхстворчатого клапана в результате декомпенсации правого желудочка выявляют набухание и пульсацию вен шеи. Также см. разделы "Стеноз устья лёгочной артерии" и "Недостаточность трёхстворчатого клапана" в главе 8 "Приобретённые пороки сердца".
Пальпация
Определяют систолическое дрожание во II межреберье слева от грудины.
Аускультация сердца
II тон при незначительном и умеренном клапанном стенозе лёгочной артерии не изменён или несколько ослаблен вследствие меньшего участия лёгочного компонента в его формировании. При выраженном стенозе и значительном увеличении давления в правом желудочке II тон может исчезать полностью. При инфундибулярном и надклапанном стенозах лёгочной артерии II тон не изменяется.
При клапанном стенозе лёгочной артерии во II межреберье слева от грудины выслушивается ранний систолический клик в момент максимального открытия створок клапана лёгочной артерии. Систолический клик усиливается при выдохе. При других уровнях стеноза (надклапанном, подклапанном) систолический клик не выслушивают.
Основное аускультативное проявление стеноза лёгочной артерии - грубый систолический шум во II межреберье слева от грудины с иррадиацией под левую ключицу и в спину. При надклапанном стенозе шум иррадиирует в левую подмышечную область и спину. Продолжительность систолического шума и его пик коррелируют со степенью стеноза: при умеренном стенозе пик шума отмечают в середине систолы, а его окончание - до аортального компонента II тона; при выраженном стенозе систолический шум более поздний и продолжается после аортального компонента II тона; при надклапанном стенозе или периферическом стенозе ветвей лёгочной артерии имеется систолический или непрерывный шум с иррадиацией в лёгочные поля.
Электрокардиография
При незначительном стенозе лёгочной артерии на ЭКГ изменений не обнаруживают. При умеренном и выраженном стенозах находят признаки гипертрофии правого желудочка. При выраженном стенозе лёгочной артерии появляются признаки гипертрофии (дилатации) правого предсердия. Возможно появление наджелудочковых аритмий.
Эхокардиография
В норме площадь клапанного отверстия лёгочной артерии 2 см 2 /м 2 . При клапанном стенозе лёгочной артерии в двухмерном режиме выявляют куполообразное выпячивание утолщённых створок клапана лёгочной артерии во время систолы правого желудочка в ствол лёгочной артерии. Характерно утолщение стенки (гипертрофия) правого желудочка. Определяют также и другие уровни обструкции лёгочной артерии и их характер. Допплеровский режим позволяет определить степень обструкции по градиенту давления между правым желудочком и лёгочным стволом. Лёгкую степень стеноза лёгочной артерии диагностируют при пиковом систолическом градиенте давления менее 50 мм рт.ст. Градиент давления 50-80 мм рт.ст. соответствует средней степени стеноза. При градиенте давления более 80 мм рт.ст. говорят о тяжёлом стенозе лёгочной артерии (градиент может достигать 150 мм рт.ст. и более в случаях выраженного стеноза).
Рентгенологическое исследование
При клапанном стенозе лёгочной артерии выявляют постстенотическое расширение её ствола. Оно отсутствует при над- и подклапанном стенозах. Характерно обеднение лёгочного рисунка.
Катетеризация полостей сердца
Катетеризация полостей сердца позволяет точно определить степень стеноза по градиенту давления между правым желудочком и лёгочной артерией.
ЛЕЧЕНИЕ И ПРОГНОЗ
Незначительный и умеренно выраженный клапанные стенозы лёгочной артерии протекают обычно благоприятно и не требуют активного вмешательства. Подклапанный мышечный стеноз прогрессирует более значительно. Надклапанный стеноз обычно прогрессирует медленно. При увеличении градиента давления между правым желудочком и лёгочной артерией более 50 мм рт.ст. при клапанном стенозе проводят вальвулопластику (после вальвулотомии у 50-60% больных развивается недостаточность клапана лёгочной артерии). При возникновении сердечной недостаточности проводят её лечение (см. главу 11 "Сердечная недостаточность"). Рекомендована профилактика инфекционного эндокардита (см. главу 6 "Инфекционный эндокардит"), поскольку риск его развития достаточно высок.
АНОМАЛИЯ ЭБШТАЙНА
Аномалия Эбштайна - расположение задней и перегородочной створок трёхстворчатого клапана у верхушки правого желудочка, приводящее к увеличению полости правого предсердия и уменьшению полости правого желудочка. Аномалия Эпштайна составляет около 1% всех врождённых пороков сердца. Возникновение данного порока связывают с поступлением лития в организм плода во время беременности.
ГЕМОДИНАМИКА
Смещение места прикрепления двух створок трёхстворчатого клапана в полость правого желудочка приводит к тому, что последний разделяется на надклапанную часть, которая объединяется с полостью правого предсердия в единую камеру (атриализация полости правого желудочка) и уменьшенную подклапанную часть (собственно полость правого желудочка) (рис. 9-8). Уменьшение полости правого желудочка приводит к снижению ударного объёма и уменьшению лёгочного кровотока. Поскольку правое предсердие состоит из двух частей (собственно правого предсердия и части правого желудочка), электрические и механические процессы в нём различаются (не сихронизированы). Во время систолы правого предсердия атриализованная часть правого желудочка находится в диастоле. Это приводит к уменьшению притока крови в правый желудочек. Во время систолы правого желудочка возникает диастола правого предсердия с неполным закрытием трёхстворчатого клапана, что приводит к смещению крови в атриализованной части правого желудочка обратно в основную часть правого предсердия. Возникает значительное расширение фиброзного кольца трёхстворчатого клапана, выраженная дилатация правого предсердия (он может вмещать более 1 л крови), повышение давления в нём и ретроградное повышение давления в нижней и верхней полых венах. Расширение полости правого предсердия и повышение в нём давления способствуют сохранению овального отверстия открытым и компенсаторному снижению давления за счёт сброса крови справа налево.

КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Больные могут предъявлять жалобы на одышку при физической нагрузке, сердцебиение из-за наджелудочковых аритмий (наблюдают у 25-30% больных и нередко служат причиной внезапной сердечной смерти).
Осмотр
Выявляют цианоз при сбросе крови справа налево, признаки недостаточности трёхстворчатого клапана (см. главу 8 "Приобретённые пороки сердца"). Характерны признаки правожелудочковой недостаточности (расширение и пульсация вен шеи, увеличение печени и отёки).
Перкуссия
Границы относительной сердечной тупости смещены вправо за счёт увеличенного правого предсердия.
Аускультация сердца
I тон сердца обычно расщеплён. Возможно появление III и IV тонов сердца. Характерен систолический шум в III-IV межреберьях слева от грудины и на верхушке за счёт недостаточности трёхстворчатого клапана. Иногда выслушивается диастолический шум сопутствующего относительного стеноза правого предсердно-желудочкового отверстия.
Электрокардиография
На ЭКГ у 20% больных могут быть выявлены признаки синдрома Вольффа-Паркинсона-Уайта (чаще имеются правосторонние дополнительные проводящие пути). Характерны признаки блокады правой ножки пучка Гиса, наличие признаков гипертрофии правого предсердия в сочетании с АВ-блокадой I степени.
Эхокардиография
Выявляют (рис. 9-9) все анатомические признаки аномалии Эбштайна: аномальное расположение створок трёхстворчатого клапана (их дистопию), увеличенное правое предсердие, правый желудочек малых размеров. В допплеровском режиме обнаруживают недостаточность трёхстворчатого клапана.

Рентгенологическое исследование
Отмечают кардиомегалию (характерна шарообразная форма тени сердца) при повышенной прозрачности лёгочных полей.
ЛЕЧЕНИЕ
При появлении симптомов сердечной недостаточности назначают сердечные гликозиды (противопоказаны при наличии синдрома Вольффа-Паркинсона-Уайта) и диуретики. Хирургическое лечение заключается в протезировании трёхстворчатого клапана или его реконструкции.
ПРОГНОЗ
Основные причины летального исхода: тяжёлая сердечная недостаточность, тромбоэмболии, абсцессы мозга, инфекционный эндокардит.
Посмотреть и купить книги по УЗИ Медведева:
Запись допплеркардиограмм используют для качественной и количественной характеристики внутрисердечных или внутрисосудистых потоков крови. Исследование митрального и аортального клапанов обычно проводят из верхушечной позиции четырехкамерного сердца.
В норме допплер-эхокардиограмма диастолического трансмитрального потока крови имеет двухфазный характер, причем спектр обоих фаз обращен к датчику - вверх выше базовой линии спектрограммы. При использовании цветного допплеровского сканирования весь спектр трансмитрального потока крови окрашивается в красные цвета. Первая фаза допплерэхокардиограммы (пик Е) обусловлена движением крови через митральный клапан во время фазы быстрого наполнения, вторая фаза (пик А) соответствует систоле ЛП. Максимальная (пиковая) скорость первой фазы (пик Е) составляет в среднем 0,62 м/ с, второй фазы (пик А) – 0,35 м/с. Соотношение максимальных скоростей потока крови в начале (пик Е) и в конце диастолы (пик А) обозначается как отношение Е/А и составляет в норме 1,5-1,7.
Систолический поток крови через аортальный клапан на допплер-эхокардио-грамме в норме имеет треугольную форму и представлен одним пиком, направленным отдатчика, т. е. вниз от базовой линии спектрограммы (при регистрации из верхушечного доступа). Пик максимальной скорости, как правило, смещен к началу потока. При использовании цветного допплеровского сканирования весь спектр трансаортального потока крови окрашивается в синий цвет.
В норме поток крови через аортальный клапан носит ламинарный характер с четко выраженным узкополостным спектром и наличием «окна» между точками с максимальной и минимальной интенсивностью.
При регистрации допплер-эхокардиограммы в импульсном режиме из верхушечного доступа контрольный (стробирующий) объем чаще устанавливают на 5-10 мм ниже аортального клапана - в выходном отделе ЛЖ(LVОТ). Перемещение контрольного (стробирующего) объема из выходного отдела ЛЖ непосредственно в область аортального клапана сопровождается появлением щелчков закрытия (в начале диастолы) и открытия (в начале систолы) створок аортального клапана. При дальнейшем перемещении контрольного объема в аорту (т.е. выше аортального клапана) щелчки исчезают. Пиковая скорость аортального потока составляет в среднем 0,96 м/с.

Исследование потока через трехстворчатый клапан лучше проводить из верхушечного доступа в позиции четырехкамерного сердца или из парастернального доступа по короткой оси на уровне сосудов основания сердца. Допплер-эхокардиограмма транстрикуспидального потока так же, как при изучении трансмитрального потока крови, располагается выше базовой линии спектрограммы и имеет двухфазный характер, причем пиковая скорость во время фазы быстрого наполнения (пик Е) не превышает в среднем 0.51 м/с, а во время систолы ПП (ник А) - 0,28 м/с. В 50-65% случаев у здоровых людей при допплер-эхокардиографии выявляется небольшой турбулентный систолический поток через трехстворчатый клапан, обусловленный физиологической регургитацией крови из ПЖ в ПП.

Исследование систолического потока через клапан легочной артерии обычно проводят из левого парастернального доступа по короткой оси. Основная волна допплеркардиограммы направлена в сторону от ультразвукового датчика и располагается ниже базовой линии спектрограммы. По сравнению с аортальным систолическим потоком крови поток в выходном отделе ПЖ и в устье ЛА меньшей амплитуды (не более 0,60-0,71 м/с) и имеет закругленную вершину. При перемещении контрольного объема из выносящего тракта ПЖ в ЛА на допплерограмме могут регистрироваться щелчки закрытия и открытия клапана ЛА.
Следует помнить, что более чем у половины здоровых лиц выявляется также небольшой диастолический поток в выносящем тракте ПЖ (регургитация крови из легочной артерии в ПЖ).

ОБЩИЙ ПЛАН УЛЬТРАЗВУКОВОГО ОБСЛЕДОВАНИЯ И АНАЛИЗА ЭХОКАРДИОГРАММ
Наиболее полные представления о морфологических и функциональных нарушениях различных структур сердца могут быть получены только при комплексном анализе одномерных, двухмерных и допплер-эхокардиограмм, зарегистрированных в различных стандартных и дополнительных позициях. Ниже приведен модифицированный протокол стандартного эхокардиографического исследования, заимствованный из монографии Н.Шиллера и М.А.Осипова (1993)
Этапы исследования Двухмерное и М-модальное исследование (датчик 3,5 МГц)
1. Парастернальный доступ (длинная ось ЛЖ).
а) двухмерный режим;
б) М-модальное исследование на уровне МК, аортального клапана и папиллярных мышц.
2. Парастернальный доступ (короткая ось ЛЖ на уровне аортального клапана):
а) двухмерный режим;
б) М-модальное исследование аорты и ЛП.
3. Парастернальный доступ (короткая ось ЛЖ на уровне створок МК)
а) двухмерное исследование;
б) М-модальное исследование.
4. Парастернальный доступ (короткая ось ЛЖ на уровне папиллярных мышц):
а) двухмерное исследование;
б) М-модальное исследование.
5. Апикальный доступ (двухмерное исследование):
а) четырехкамерная позиция - оптимальная визуализация ЛЖ, ЛП, ПЖ, ПП;
б) «пятикамерная» позиция;
в) двухкамерная позиция - оптимальная визуализация ЛЖ, ЛП;
г) по длинной оси ЛЖ.
6. Субкостальный доступ (двухмерное исследование):
а) позиция подлинной оси сердца;
б) позиция по короткой оси основания сердца;
в) позиция по короткой оси ЛЖ на уровне митрального клапана;
г) позиция подлинной оси нижней полой вены;
д) позиция подлинной оси брюшной аорты.
7. Супрастернальный доступ (двухмерное исследование):
а) позиция подлинной оси дуги аорты;
б) позиция по короткой оси дуги аорты.
Допплеровское исследование (датчик 2,5 МГц)
Парастернальный доступ (длинная ось ЛЖ):
а) запись кровотока в выносящем тракте ЛЖ;
б) поиск патологических потоков и их регистрация.
2. Парастернальный доступ (короткая ось ЛЖ на уровне аортального клапана): а) регистрация кровотока в ЛА в импульсном и постоянно-волновом режимах;
3. Апикальный доступ (четырехкамерная позиция):
а) регистрация трансмитрального кровотока в импульсном режиме;
б) при наличии митральной регургитации - регистрация ее в постоянно-волновом режиме.
4. Апикальный доступ («пятикамерная» позиция):
а) запись кровотока в выносящем тракте ЛЖ в импульсном и постоянно-волновом режимах.
5. Апикальный доступ (четырехкамерная позиция):
а) при наличии трикуспидальной регургитации - запись ее в постоянно-волновом режиме.
ОЦЕНКА СИСТОЛИЧЕСКОЙ ФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА
Систолическая функция ЛЖ оценивается по нескольким показателям, центральное место среди которых занимает ударный объем (УО) и фракция выброса (ФВ).
1. Метод Teicholz . До последнего времени расчет УО, ФВ и других гемодинамических показателей проводился на основании измерений М - модальной эхокардиограммы, зарегистрированной из левого парастернального доступа. Для расчета учитывается степень передне-заднего укорочения ЛЖ, то есть отношения КДР и KCР Расчет проводится по формуле L.Teicholz:

где V - объем ЛЖ (КСО или КДО) и D - переднезадний размер ЛЖ в систолу или диастолу. УО определяется как разница КДО и КСО, а ФВ - как отношение УО к КДО.
В настоящее время большинство исследователей отказались от такого способа определения гемодинамических показателей, поскольку расчет КДО и КСО ЛЖ, согласно этой методике, основан на измерении КДР и КСР лишь небольшой части ЛЖ у его основания и не учитывает всей сложной геометрии полости желудочка. Способ Teicholz не пригоден также для определения УО у большинства больных ИБС, у которых имеются локальные очаговые нарушения сократимости ЛЖ. Это требует от практического врача весьма осторожного отношения к этим измерениям и расчетам.

2. Метод дисков (модифицированный метод Simpson). Существенно более точные результаты вычисления глобальной сократимости ЛЖ могут быть получены при количественной оценке двухмерных эхокардиограмм. Наиболее пригоден для этой цели метод Simpson (метод дисков), основанный на планиметрическом определении и суммировании площадей 20 дисков, представляющих собой своеобразные поперечные срезы ЛЖ на разных уровнях. Для расчета систолических и диастолических объемов ЛЖ получают два взаимоперпендикулярных двухмерных изображения сердца из верхушечного доступа в позициях двухкамерного и четырехкамерного сердца. После выделения курсором в обеих проекциях внутреннего контура ЛЖ последний автоматически делится на 20 дисков (а и Ь) одинаковой высоты и вычисляется их площадь (S):
Для расчета объема ЛЖ (V) площади 20 дисков суммируются, и сумма умножается на высоту каждого диска ЛЖ (L/20):
где L - длина ЛЖ.
Так получают значения КДО и КСО.

3. Метод «площадь-длина». При отсутствии региональных нарушений сократимости может быть использован еще один простой метод определения УО с помощью двухмерной эхокардиографии. На эхокардиограмме четырехкамерного или двухкамерного сердца, зарегистрированной из верхушечного доступа, планиметрический определяют площадь полости ЛЖ (А) и его длину (L). Объем ЛЖ (V) определяют по формуле:
где А - площадь ЛЖ на изображении и L - длина полости ЛЖ.
Дальнейший расчет гемодинамических показателей проводится по классическим формулам:

где МО - минутный объем, УИ - ударный индекс, СИ - сердечный индекс, S - площадь поверхности тела, определяемая по специальным номограммам.

4. Метод допплер-ЭхоКГ . Определение УО, ФВ и других гемодинамических показателей с помощью допплер-ЭхоКГ основано на измерении величины объемного кровотока через аортальный клапан. С этой целью из верхушечного доступа в позициях двухкамерного или пятикамерного сердца проводят допплер-локацию выходного отдела ЛЖ в импульсном режиме, устанавливая контрольный объем в центре выходного тракта на 10 мм проксимальнее закрытых створок аортального клапана, и получают систолический спектр линейной скорости кровотока в выходном отделе ЛЖ. При этом автоматически рассчитывают среднюю линейную скорость кровотока (V) и интеграл линейной скорости кровотока (LVOT VTI), т.е. сумму всех моментных значений линейной скорости во время изгнания крови в аорту. Последний можно представить также как произведение Vcp (м/с) на длительность периода изгнания (ЕТ) в секундах: LVOT VTI = Vcp ЕТ (см).
После этого в режиме двухмерной ЭхоКГ, зарегистрированной из парастернального доступа по длинной оси ЛЖ, в середине систолы измеряют внутренний диаметр фиброзного кольца аортального клапана (D), автоматически рассчитывая площадь поперечного сечения корня аорты. Для расчета УО (мл) интеграл линейной скорости кровотока умножают на площадь поперечного сечения аорты – Sao.
Понятно, что то же значение УО может быть получено при умножении средней линейной скорости кровотока на продолжительность систолы (ЕТ, в с) и площадь поперечною сечения аорты:

ОЦЕНКА ДИАСТОЛИЧЕСКОЙ ФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА
I Диастолическую функцию ЛЖ оценивают по результатам исследования трансмитрального диастолического кровотока в импульсном допплеровском режиме.
Определяют:
1) максимальную скорость раннего пика диастолического наполнения (Vmax Peak E);
2) максимальную скорость трансмитрального кровотока во время систолы левого предсердия 1 (Vmax Peak A);
3) площадь под кривой (интеграл скорости) раннего диастолического наполнения (MVVTI Peak E)
4) предсердной систолы (MV VTI Peak A);
5) отношение максимальных скоростей (или интегралов скорости) раннего и позднего наполнения (Е/А);
6) время изоволюмического расслабления ЛЖ - IVRT (измеряется при одновременной регистрации аортального и трансмитрального кровотока в постоянно-волновом режиме из апикального доступа);
7) время замедления раннего диастолического наполнения (DT).

В норме диастолический поток крови через митральный клапан при регистрации в допплеррсжиме имеет двухволновую форму. После открытия митрального клапана скорость потока крови через левое атриовентрикулярное отверстие быстро увеличивается до максимальной и затем так же быстро уменьшается почти до нулевой линии. Этот ранний диастолический пик (Peak E) соответствует фазе быстрого наполнения ЛЖ и в норме составляет около 0,62 м/с. Время изоволюмического расслабления ЛЖ(IVRT), представляющее собой интервал между окончанием потока в выходном тракте ЛЖ и началом потока через митральный клапан, является хорошим показателем скорости начальной релаксации желудочка. В норме IVRT ЛЖ составляет не более 70-75 мс, а время замедления раннего диастолического наполнения (DT) - 200 мс.
В конце диастолы во время сокращения ЛП скорость потока крови снова увеличивается, образуя второй пик (Peak А), и затем возвращается к нулевой линии, когда митральный клапан закрывается. При нормальной диастолической функции на допплерограмме преобладает пик раннего диастолического наполнения (Peak Е), который в 1,5-1,6 раза выше пика позднего наполнения желудочка (Peak A).

| Vmax Peak E | Vmax Peak A | Е/А | IVRT | DT |
| 0,62 м/с | 0,35 м/с | 1,5-1,6 | 70-75 мс | 200 мс |
ДИАСТОЛИЧЕСКАЯ ДИСФУНКЦИЯ ЛЕВОГО ЖЕЛУДОЧКА
Начальные стадии нарушения диастолической функции ЛЖ, не сопровождающиеся увеличением КДД в желудочке и давления в ЛП, характеризуются снижением скорости изоволюмического расслабления и объема раннего диастолического наполнения. При этом объем ЛП непосредственно перед началом его сокращения, т.е. в конце диастолы, заметно увеличивается. Результатом этого по закону Франка-Старлинга является более сильное сокращение ЛП и увеличение фракции предсердного наполнения (пика А). Иными словами, на начальной стадии развития диастолической дисфункции замедление релаксации ЛЖ приводит к перераспределению диастолического наполнения в пользу предсердного компонента и значительная часть диастолического кровотока осуществляется во время активной систолы ЛП.
На допплерограммах трансмитрального кровотока выявляется снижение амплитуды пика Е и увеличение высоты пика А. Отношение Е/А уменьшается до 1,0 и ниже. Одновременно определяется увеличение времени изоволюмического расслабления ЛЖ (IVRT) больше 90-100 мс и времени замедления раннего диастолического наполнения (DT) - больше 220 мс.

Такой тип диастолической дисфункции ЛЖ получил название типа «замедленной релаксации» . Наиболее частыми факторами, ведущими к формированию данного типа диастолической дисфункции ЛЖ являются хроническая или транзиторная ишемия миокарда у больных ИБС, кардиосклероз любого генеза (в том числе постинфарктный), гипертрофия миокарда, поражения перикарда, блокады! ножек пучка Гиса и др.
Дальнейшее прогрессирование нарушений внутрисердечной гемодинамики приводит к росту давления в ЛП и увеличению предсердно-желудочкового градиента давления во время фазы быстрого наполнения. Это сопровождается значительным ускорением раннего диастолического наполнения желудочка (Peak E) при одновременном уменьшении скорости кровотока во время систолы предсердия (Peak А). Рост конечно-диастолического давления в ЛЖ способствует еще большему ограничению кровотока во время предсердной систолы. Происходит своеобразная патологическая «псевдонормализация» диастолического наполнения ЛЖ с увеличением значений максимальной скорости раннего диастолического наполнения (Peak E) и уменьшением скорости предсердного наполнения (Peak А). В результате отношение Е/А увеличивается больше 1,6- 1,8. Эти изменения сопровождаются укорочением фазы изоволюмического расслабления (IVRT) меньше 70 мс и времени замедления раннего диастолического наполнения (DT) меньше 150 мс.

Такой, «рестриктивный » тип диастолической дисфункции, как правило, наблюдается при застойной СН, свидетельствуя о повышении давления наполнения ЛЖ. Нередко описанные признаки диастолической дисфункции ЛЖ предшествуют нарушениям его систолической функции, причем «рестриктивный» тип является прогностически менее благоприятным.
Диастолическая дисфункция ЛЖ у больных с ХСН и сохранной систолической функцией характеризуется соответствующими патологическими значениями параметров, на которых основывается диагностика этого типа ХСН. Допплер-ЭхоКГ критерии нарушения диастолической функции ЛЖ у больных с ХСН с сохранной систолической функцией представлены в таблице 6.
Таблица 6. Эхокардиографические критерии диастолической дисфункции ЛЖ у больных с ХСН .
|
Параметры |
Патологические признаки |
Клинические симптомы |
|
Снижен (< 8 см/с от септальной стенки, <10 см/с от латеральной и < 9 см/с среднее |
Замедленная релаксация ЛЖ |
|
|
Высокое (>15) | ||
|
Низкое (<8) | ||
|
Промежуточное (8-15) |
Серая зона (необходимы дополнительные параметры) |
|
|
трасмитрального кровотока |
Рестриктивный тип (>2) |
Высокое давление наполнения ЛЖ |
|
Объемная перегрузка |
||
|
Замедленная релаксация (<1) |
Замедленная релаксация ЛЖ |
|
|
Нормальное давление наполнения ЛЖ |
||
|
Нормальный (1-2) |
Неокончательно (возможна «псевдонормализация») |
|
|
Трансмитральный кровоток при пробе Вальсальвы |
Переход псевдонормального типа в замедленную релаксацию (со снижением Е/А ≥ чем на 0,5) |
Повышенное давление наполнения ЛЖ |
|
(А pulm – A mitr) продолжительность |
Высокое давление наполнения |
Примечание: А pulm – A mitr = разница между длительностью пиков А в легочных венах и А – трансмитрального потока; Е/е´ - отношение трансмитрального Е пика к тканевому миокардиальному допплеровскому е´ (ТМД); Е/А – соотношение между пиками трансмитрального кровотока; ХСН – хроническая сердечная недостаточность; ЛЖ – левый желудочек;
Известно, что нормальные величины ЭхоКГ показателей при функциональной диастолической дисфункции ЛЖ зависят от возраста, ЧСС и площади поверхности тела. Важно отметить, что нет одного единственного высокочувствительного ЭхоКГ критерия, на котором основывается диагностика диастолической дисфункции ЛЖ. Необходимо проведение подробного ЭхоКГ протокола, включающего двумерную ЭхоКГ, допплер-ЭхоКГ и ТМД. Оцениваются структурные (гипертрофия ЛЖ, дилатация ЛП) и функциональные показатели. ТМД используется для измерения скорости раннего диастолического пика (е´) от кольца митрального клапана, характеризующего миокардиальную релаксацию. Нормальное значение е´ (> 8 см/с от септальной стенки, > 10 см/с от латеральной и > 9 см/с среднее - при измерении в реальном времени импульсного режима ТМД) крайне редко встречается у больных с ХСН. Доказано, что отношение Е/е´ коррелирует с давлением наполнения ЛЖ. Таким образом, к эхокардиографическим критериям диастолической дисфункции ЛЖ относятся: снижение показателя е´ (е´ средний < 9 см/с), увеличение соотношения Е/е´ (>15), а также комбинация некоторых показателей. Наличие двух патологических критериев и/или фибрилляция предсердий повышают вероятность диагноза.
Методические аспекты применения Допплер-эхокардиографии в диагностике диастолической дисфункции левого желудочка
А.Г. Овчинников, Ф.Т. Агеев, В.Ю. Мареев
НИИ кардиологии им. А.Л. Мясникова (дир. - акад. РАМН Ю.Н. Беленков) РК НПК Минздрава РФ, Москва
URL
В настоящее время доказано, что признаки диастолической дисфункции встречаются практически при любом заболевании сердца. Считается, что снижение систолической функции сердца всегда сопровождается хотя бы минимальными нарушениями диастолической функции левого желудочка (ЛЖ) . Более того, существуют данные, что нарушения диастолических свойств миокарда обычно предшествуют снижению насосной функции ЛЖ и даже могут изолированно приводить к появлению признаков и симптомов хронической сердечной недостаточности (ХСН) . В настоящее время доказано, что примерно у 30-40% больных ХСН систолическая функция ЛЖ остается нормальной или малоизмененной , т.е. в основе синдрома ХСН у таких больных, по-видимому, лежат диастолические расстройства. Установлено, что больные с диастолической сердечной недостаточностью (СН) имеют более благоприятный прогноз, чем пациенты с систолической СН (уровень годичной летальности составляет 8 и 19% соответственно ). А с учетом имеющихся особенностей в тактике ведения этой категории больных ХСН становится понятной актуальность выявления диастолической дисфункции ЛЖ. Так, Американская ассоциация сердца рекомендует проводить оценку как систолической, так и диастолической функции ЛЖ у каждого больного с впервые возникшими симптомами ХСН . Поскольку клинические признаки диастолической и систолической СН во многом схожи , решающую роль в оценке диастолической функции ЛЖ приобретают визуализирующие методы диагностики, и в первую очередь эхокардиография. В свое время для оценки диастолической функции ЛЖ был предложен ряд способов, основанных на М-модальном и двумерном эхо-исследовании , не получивших, однако, большой распространенности из-за присущих им значимых погрешностей в оценке получаемых результатов. Более 15 лет прошло с того момента, как впервые было показано, что спектр трансмитрального диастолического потока, получаемый при импульсно-волновом Допплеровском исследовании весьма точно отражает динамику диастолического наполнения ЛЖ . С тех пор этот метод получил всеобщее признание и в настоящее время является ведущим неинвазивным методом оценки диастолической функции ЛЖ. В данном обзоре будут освещены возможности Допплер-эхокардиографии в выявлении диастолических нарушений, перечислены присущие данной методике ограничения и описаны способы их преодоления.
Рис.1 Временная диаграмма периодов и фаз диастолы. Условные обозначения: АС - атриальная систола; БН - фаза быстрого наполнения; ИВР - изоволюметрическое расслабление; МН - фаза медленного наполнения; Ao - динамика давления в выносящей аорте; LA - динамика давления в ЛП; LV-динамика давления в ЛЖ. Взято из:.

Рис.2. Влияние изменений податливости ЛЖ на тип трансмитрального диастолического спектра. Вверху: уменьшение податливости ЛЖ приведет к увеличению пика Е и укорочению DT трансмитрального диастолического спектра. В основе подобных изменений может лежать один из следующих механизмов. Внизу слева:увеличение объема ЛЖ сместит петлю давление-объем вправо (пунктирная линия) вдоль неизмененной кривой давление-объем (сплошная линия). Внизу справа: при повышении жесткости самого миокарда происходит смещение петли давление-объем вверх и влево (стрелки).

Рис. 3. Трансмитральный диастолический спектр. Условные обозначения: Е - максимальная скорость пика Е; А - максимальная скорость пика А; ИВР - время изоволюметрического расслабления; DT - время замедления кровотока раннего диастолического наполнения ЛЖ; II - второй тон сердца.

Рис. 4. Динамика давлений в ЛЖ и ЛП и тип трансмитрального диастолического спектра у здоровых лиц и у пациентов с диастолическими нарушениями разной степени тяжести. Взято из: .

Рис. 5. Динамика трансмитрального и легочного венозного спектров по мере прогрессирования диастолических нарушений. Обратите внимание, что антеградная диастолическая волна легочного потока повторяет характер изменений пика Е трансмитрального спектра (стрелки). Условные обозначения: ИВР - время изоволюметрического расслабления; PVS - систолический антеградный поток спектра легочных вен; PVD - диастолический антеградный поток спектра легочных вен; PVa - диастолический ретроградный поток спектра легочных вен. Взято из: .
Краткая физиология диастолы
Под нормальной
диастолической функцией подразумевается способность ЛЖ "принимать"
в себя количество крови, необходимое для поддержания сердечного
выброса при среднем венозном легочном давлении, не превышающем
12 мм рт. ст. . Диастолу подразделяют на 4 дискретных периода
(рис. 1): 1) изоволюметрического расслабления; 2) быстрого раннего
заполнения; 3) медленного заполнения (или диастазиса) и 4) сокращения
предсердий . Диастола представляет собой чрезвычайно сложный
процесс, который находится под влиянием множества взаимодействующих
друг с другом факторов, определяющих в конечном счете сопротивление
заполнению ЛЖ . Из целого ряда детерминант заполнения ЛЖ
основными являются активное расслабление ЛЖ и податливость ЛЖ.
Изменение любого из этих компонентов может привести к возрастанию
сопротивления наполнению ЛЖ и соответствующему повышению давления
наполнения (с целью поддержания необходимого конечного диастолического
объема ЛЖ), т.е. к нарушению диастолы.
Таблица. Значения показателей различных типов трансмитрального
диастолического и легочного венозного спектров
| Пациент (>65 лет) | Норма | Нарушение релаксации | Псевдонормализация | Рестрикция | |
| Митральный спектр | E/A
і
> 0/75 DT=160-240 мс |
E/A < 0/75 DT >240 мс |
E/A >1 DT > 160 мс |
E/A >>1 DT < 160 мс |
|
| Спектр легочных вен | S > D PV A dur < MV A dur |
S >> D PV A dur < MV A dur |
S < D PV A dur > MV A dur |
S < D PV A dur > MV A dur |
|
| Условные обозначения: А - максимальная скорость пика А трансмитрального спектра; D - диастолический антеградный поток спектра легочных вен; DT - время замедления пика Е; Е - максимальная скорость пика Е трансмитрального спектра; MV A dur - продолжительность волны А митрального диастолического спектра; PV A dur - продолжительность диастолического ретроградного потока спектра легочных вен; S - систолический антеградный поток спектра легочных вен. Взято из: . | |||||
Расслабление миокарда ЛЖ начинается во вторую половину систолы, захватывает период изоволюметрического расслабления и оканчивается в фазу раннего диастолического наполнения. Это энергетически зависимый процесс, связанный с активным поступлением ионов Ca 2+ в саркоплазматический ретикулум кардиомиоцита. Скорость миокардиальной релаксации определяется :
- инотропным статусом ЛЖ (так, катехоламины усиливают активную релаксацию, а повышение концентрации внутриклеточного Ca 2+ замедляет этот процесс);
- степенью нагрузки на ЛЖ во время изгнания крови (повышение постнагрузки на ЛЖ замедляет релаксацию);
- ЧСС (повышение ЧСС ускоряет релаксацию);
- синхронностью сокращения и расслабления миокарда ЛЖ.
Скорость, с которой
во время расслабления происходит снижение давления в полости ЛЖ,
зависит от скорости релаксации и феномена “эластической отдачи”.
Феномен “отдачи” (или “присасывания”) происходит благодаря растяжению
эластических элементов, подвергшихся сжатию во время предшествующей
систолы. При снижении систолической функции ЛЖ возрастает конечный
систолический объем ЛЖ и соответственно уменьшается вклад эластической
отдачи в заполнение ЛЖ.
Податливость ЛЖ
- пассивная функция сердца,
отражающая растяжимость камеры ЛЖ во время его заполнения .
Пассивные свойства миокарда начинают определять заполнение ЛЖ
уже в период ранней диастолы, но максимально влияют на процесс
наполнения в фазу диастазиса и систолы предсердий. Податливость
миокарда определяется прежде всего свойствами самого миокарда
(миокардиальная податливость
). Такие патологические процессы,
как гипертрофия, фиброз, или инфильтрация миокарда снижают его
растяжимость во время диастолического заполнения ЛЖ, что приводит
к более крутому наклону кривой давление-объем диастолического
заполнения ЛЖ (т.е. для увеличения объема ЛЖ в диастолу на единицу
объема потребуется большее давление заполнения (рис. 2, левая
часть). Кроме того, податливость миокарда зависит и от уровня
преднагрузки ЛЖ (податливость камеры
). Поскольку кривая
давление-объем имеет экспоненциальный характер, при увеличении
объема (преднагрузки) связь давление-объем сместится вдоль кривой
вправо, т.е. к более крутой ее порции (рис. 2, правая часть).
Таким образом, при увеличении растяжения ЛЖ (дилатации) он становится
менее податливым (или более жестким). Другими, менее значимыми
факторами, влияющими на податливость ЛЖ, являются перикардиальное
ограничение , межжелудочковое взаимодействие , тургор
коронарных артерий и ряд других.
Трансмитральный диастолический спектр в норме
Для получения
скоростного спектра трансмитрального потока контрольный объем
импульсно-волнового Допплеровскоо режима следует размещать над
местом смыкания створок митрального клапана. Именно в этой позиции
контрольного объема будут регистрироваться максимальные скорости
. Следует помнить о том, что допплеровские кривые демонстрируют
лишь характер заполнения
ЛЖ, который может варьировать
под воздействием не только изменений собственно диастолических
свойств ЛЖ, но и нагрузочных условий заполнения камер сердца и,
таким образом, лишь косвенно
отражают особенности функционирования
сердца в диастолу.
Для оценки диастолической функции ЛЖ в свое
время предлагалось множество параметров диастолического трансмитрального
спектра, однако в настоящее время с этой целью в основном используются
следующие (рис.3): максимальная скорость раннего пика Е, максимальная
скорость предсердной систолы А, соотношение Е/А, время замедления
кровотока
раннего диастолического наполнения ЛЖ, время изоволюметрического
расслабления ЛЖ. Время замедления пика Е (DT, deceleration time)
представляет собой временной интервал от момента достижения максимума
скорости пика Е до момента пересечения нисходящего участка волны
Е с нулевым уровнем . В случае, если волна А возникает прежде,
чем пик Е достигнет нуля и, таким образом, наслаивается на конечную
часть пика Е, необходимо экстраполировать контур нисходящего колена
пика Е до нулевого уровня (см. рис.3). Время изоволюметрического
расслабления ЛЖ (ИВР), может быть рассчитано как интервал от клика
закрытия аортального систолического потока до начала трансмитрального
диастолического потока при одновременной их регистрации с помощью
постоянно-волнового Допплеровского исследования , а также
от начала II тона фонокардиограммы до клика открытия митрального
клапана импульсно-волнового Допплера.
Теперь вкратце рассмотрим гемодинамическую значимость
указанных параметров.
Время ИВР ЛЖ.
Хотя продолжительность
ИВР ЛЖ определяется скоростью релаксации миокарда ЛЖ, следует
помнить о зависимости этого показателя от нагрузочных условий;
так, при исходно одинаковой скорости релаксации время ИВР возрастет
при повышении давления в аорте (за счет более раннего захлопывания
створок аортального клапана) и уменьшится при возрастании
давления в левом предсердии - ЛП (раньше откроется митральный
клапан).
Пик Е.
Контур волны Е трансмитрального
спектра отражает изменения градиента давлений между ЛП и ЛЖ в
период раннего диастолического наполнения ЛЖ. На величину этого
градиента оказывают влияние скорость и степень релаксации ЛЖ,
и давление в ЛП в момент открытия митрального клапана. Поэтому
низкие значения пика Е могут быть обусловлены как снижением давления
в ЛП (например, при
уменьшении
венозного возврата к сердцу), так и нарушением расслабления ЛЖ,
приводящего к замедлению снижения давления в ЛЖ в раннюю диастолу.
Наоборот, возрастание пика Е может свидетельствовать как о повышении
давления в ЛП, так и об ускорении процесса релаксации (например,
под действием катехоламинов).
DT.
Наконец, давление в ЛЖ достигает своего минимума и под действием
поступающей в полость ЛЖ крови начинает повышаться, что приведет
к снижению градиента давлений ЛП-ЛЖ. Скорость снижения этого градиента
определяется временем замедления кровотока раннего диастолического
наполнения ЛЖ (DT). Так, замедление миокардиальной релаксации
приведет к недозаполнению полости ЛЖ в раннюю диастолу (через
снижение раннего градиента давлений между ЛП и ЛЖ), что обусловит
медленное последующее возрастание давления в ЛЖ и соответственно
удлинение DT. Наоборот, при увеличении жесткости миокарда давление
в полости ЛЖ быстро возрастает и DT укорачивается.
Пик А.
Примерно к середине диастолы происходит
выравнивание давлений в ЛП и ЛЖ (фаза диастазиса), и кровоток
через митральный клапан практически отсутствует вплоть до систолы
предсердий (пика А). Величина пика А зависит от преднагрузки ЛП
(его наполнения к моменту предсердного сокращения) и жесткости
миокарда ЛЖ.
Типы трансмитрального спектра в зависимости от тяжести диастолических нарушений
В зависимости
от тяжести диастолических нарушений выделяют следующие типы трансмитрального
диастолического спектра: 1) спектр с нарушенным расслаблением
ЛЖ; 2) "псевдонормальный" спектр и 3) рестриктивный спектр .
Интересно, что тип трансмитрального спектра отражает лишь степень
тяжести имеющихся диастолических нарушений, но не является специфичным
для того или иного заболевания сердца. Характер спектра может
меняться как по мере прогрессирования диастолических нарушений,
так и под действием лечения. Рассмотрим коротко патофизиологическую
основу каждого типа спектра.
Спектр с нарушенным расслаблением ЛЖ
(рис.
4). Считается, что нарушения релаксации возникают уже на самых
ранних стадиях большинства сердечных заболеваний, когда систолическая
функция ЛЖ еще остается сохраненной, а имеющиеся незначительные
диастолические нарушения не способны вызывать вторичных адаптивных
изменений со стороны гемодинамики . Кроме того,
данный
спектр характерен для лиц пожилого возраста , у которых
он является отражением всего лишь возрастных изменений миокарда,
а не какого-либо патологического процесса. В норме акцент заполнения
ЛЖ приходится на фазу раннего заполнения: 60-80% конечно-диастолического
объема крови успевает "перетечь" в ЛЖ к моменту систолы предсердий,
сокращение предсердий имеет незначительное влияние на общее заполнение
ЛЖ. При замедлении расслабления ЛЖ кровь в раннюю диастолу поступает
в ЛЖ в ограниченном объеме
.
Это приведет к скоплению избыточного количества крови в ЛП к моменту
его систолы, что через механизм Франка-Старлинга увеличит силу
предсердного сокращения (величины пика А). При нарушенной релаксации
происходит замедление скорости раннедиастолического падения давления
в ЛЖ, что отразится на удлинении времени ИВР и уменьшении пика
Е. Кроме того, уменьшение наполнения ЛЖ (и соответственно опорожнения
ЛП) в раннюю диастолу приведет к более позднему выравниванию давлений
в ЛП и ЛЖ (увеличится DT), а акцент наполнения ЛЖ сместится на
систолу предсердий (увеличение пика А) . За счет более энергичного
сокращения ЛП (механизм Франка-Старлинга) общее диастолическое
наполнение ЛЖ поддерживается на нормальном уровне без сопутствующего
повышения венозного легочного давления.
"Псевдонормальный" спектр
(см. рис. 4).
При прогрессировании заболевания наблюдается не только дальнейшее
ухудшение процессов расслабления, но и происходит снижение податливости
стенок ЛЖ. В эту стадию механизм "предсердной подкачки" уже не
в состоянии самостоятельно обеспечивать необходимое наполнение
ЛЖ, и сердечный выброс может быть сохранен только путем повышения
легочного венозного давления. При этом включаются компенсаторные
механизмы (веноконстрикция и задержка натрия), направленные на
повышение давления в легочных венах и ЛП, что приведет в свою
очередь к появлению признаков венозного застоя в легких. Повышенное
давление в ЛП будет "стремиться" увеличить объем раннего диастолического
наполнения, что приведет к "нормализации" трансмитрального градиента
давления в раннюю диастолу - уменьшится время ИВР, а величина
пика Е вновь вернется к норме. За счет возросшей жесткости ЛЖ
будет наблюдаться более крутое повышение давления в его полости,
что повлечет за собой укорочение DT. Кроме того, заметное повышение
диастолического давления в ЛЖ к моменту предсердной систолы увеличит
пост-нагрузку на ЛП, что приведет к уменьшению значимости ЛП как
"подкачки" - произойдет снижение пика А. Следовательно, при выраженных
нарушениях диастолы и заметном увеличении давления в ЛП, несмотря
на присутствие выраженных нарушений расслабления ЛЖ, трансмитральный
спектр может приобретать вид нормального - происходит его "псевдонормализация".
Рестриктивный спектр
(см. рис. 4). Последующее
увеличение жесткости ЛЖ будет сопровождаться дальнейшим повышением
давления в ЛП. В раннюю диастолу кровь попадает в малоподатливый
ЛЖ, что будет сопровождаться крутым подъемом давления в ЛЖ. Это
приведет к еще большему укорочению DT. Помимо этого, резко возрастает
сопротивление
опорожнению
ЛП в предсердную систолу со стороны ригидного ЛЖ, поэтому пик
А будет значительно уменьшен или даже может не определяться.
Дифференциация истинно нормального трансмитрального диастолического спектра от псевдонормального
В отличие от спектра
с нарушенным расслаблением или рестриктивного спектра, имеющих
весьма специфичные отличительные признаки (см. таблицу), существуют
значительные трудности в дифференциации нормального трансмитрального
диастолического спектра от псевдонормального. Вместе с
тем "нормальная" форма трансмитрального
спектра может указывать как на отсутствие каких-либо диастолических
нарушений (в случае истинно нормального спектра), так и на значительно
выраженную миокардиальную патологию (в случае "псевдонормализации")
и, следовательно, на необходимость медикаментозной коррекции.
Естественно, наличие клинических признаков значимой дисфункции
ЛЖ с большей вероятностью будет свидетельствовать о повышении
давления наполнения ЛЖ, чем об отсутствии диастолических нарушений.
Однако далеко не всегда удается лишь на основании клинической
картины разграничить эти два спектра друг от друга. К настоящему
времени существует несколько способов, позволяющих производить
подобную дифференциацию.
Анализ венозного легочного спектра.
Спектр
легочного венозного потока можно получить, располагая контрольный
объем на 1-2 см проксимальнее места впадения правой верхней легочной
вены в ЛП. При трансторокальной эхокардиографии приемлемый для
анализа спектр удается получить примерно в 90% случаев . В
норме легочный спектр состоит из
систолического и диастолического антеградных и диастолического
ретроградного скоростных потоков (рис. 5). Последний возникает
при предсердном сокращении (волна А), когда кровь перемещается
как в полость ЛЖ, так и забрасывается обратно в легочные вены.
То, в каком направлении будет перемещаться кровь в систолу предсердий,
зависит от уровня постнагрузки ЛП (степени податливости ЛЖ). При
существенном возрастании давления в ЛЖ к моменту систолы предсердий,
что наблюдается при "псевдонормализации", начинает преобладать
ретроградный ток крови в систему легочных вен, что приведет к
укорочению волны А трансмитрального спектра и увеличению скорости
и продолжительности волны А венозного легочного спектра (см. рис.
5). Так, выявление максимальной скорости легочной волны А >
35 см/с и превышение продолжительности волны А митрального
спектра укажет на существенное повышение жесткости ЛЖ и,
таким образом, позволит распознать "псевдонормализацию". Установлено,
что если разница по продолжительности превышает 30 мс, конечное
диастолическое давление окажется более 15 мм рт. ст. с чувствительностью
85% и специфичностью 79% . Кроме того, анализ антеградных
компонентов легочного венозного спектра также позволяет судить
о наличии или отсутствии "псевдонормализации". Систолический поток
отражает наполнение ЛП во время систолы желудочков, а диастолический
антеградный поток совпадает по времени с ранним диастолическим
наполнением ЛЖ и соответствует пику Е трансмитрального спектра.
При повышении жесткости миокарда ЛЖ (и сопутствующем повышении
давления в полости ЛП) акцент заполнения ЛП сместится на период
ранней диастолы, что на кривой легочного потока отразится в виде
снижения скорости систолической волны и повышения скорости антеградной
диастолической волны. Критериями "псевдонормализации" будут являться:
1) максимальная скорость антеградной диастолической волны >
60 см/с; 2) соотношение пиков систолического и диастолического
антеградного потоков < 75%. Однако следует заметить, что при
наличии сохраненной систолической
функции ЛЖ не всегда будет наблюдаться снижение систолической
антеградной волны. Это обстоятельство снижает чувствительность
данных критериев до 60% .
Маневр Вальсальвы.
В норме снижение венозного
возврата к сердцу (что наблюдается во время фазы напряжения маневра
Вальсальвы) приведет к уменьшению амплитуды как волны Е, так и
волны А трансмитрального спектра и, таким образом, соотношение
E/A останется практически неизменным. Однако диастолическая дисфункция
на стадии "псевдонормализации" трансмитрального спектра проявляется
помимо повышения жесткости миокарда ЛЖ и выраженными нарушениями
релаксации ЛЖ. Поэтому снижение повышенного давления в ЛП на фоне
уменьшения возврата к сердцу приведет к снижению раннедиастолического
градиента давлений между ЛП и ЛЖ, что создаст предпосылки для
демаскировки имеющихся нарушений релаксации: будет наблюдаться
выраженное снижение пика Е при отсутствии уменьшения амплитуды
волны А c соответствующим уменьшением соотношения Е/А .
Динамика внутрижелудочкового диастолического
потока.
Установлено, что у здоровых лиц смещение контрольного
объема на 2-3 см от края створок митрального клапана внутрь полости
ЛЖ по направлению к верхушке не вызовет значимых изменений амплитуды
пика Е. При выраженной диастолической дисфункции ЛЖ, однако, наблюдается
немедленное снижение пика Е . Имеются сообщения об использовании
М-модального цветного Допплеровского исследования, с помощью которого
также можно оценить динамику внутрижелудочкового диастолического
потока. Так, у пациентов с нарушенной релаксацией ЛЖ наклон раннего
диастолического потока будет более пологим по сравнению с нормой
. Кроме того, в случае нарушенного расслабления временной
интервал между достижением максимума волны Е у края створок митрального
клапана и на верхушке сердца окажется увеличенным . Эти признаки
сохраняются и при "псевдонормализации" трансмитрального спектра
.
Заключение
Допплер-эхокардиография позволяет осуществлять не только качественную диагностику диастолических нарушений, но и определять степень их тяжести. При прогрессировании сердечного заболевания характер трансмитрального Допплеровского спектра претерпевает сложные изменения, связанные как с усугублением диастолических нарушений, так и с развитием гемодинамических приспособительных реакций, действующих через повышение давления в ЛП и/или конечного диастолического давления ЛЖ и приводящих к формированию псевдонормального и рестриктивного трансмитрального спектра. Выявление этих типов спектров имеет важное клиническое значение, поскольку указывает на выраженные диастолические расстройства и, следовательно, на необходимость их медикаментозной коррекции. Существуют определенные сложности в разграничении истинно нормального трансмитрального спектра от псевдонормального, однако существует ряд способов решения этой проблемы.
Литература:
1. Nishimura R.A., Tajik A.J. Evaluation of
diastolic filling of left ventricle in health and disease: Doppler
echocardiography is the clinician"s Rosetta Stone
.
J Am Coll Cardiol 1997;30:8-18.
2. Ohno M., Cheng C.P., Little W.C. Mechanism
of altered patterns of left ventricular filling during the development
of congestive heart failure. Circulation 1994;89:2241-50.
3. Labovitz A.J., Pearson A.C. Evaluation of
left ventricular diastolic function: clinical relevance and recent
Doppler echocardiographic insights. Am Heart J 1987;114:836-51.
4. Brutsaert D.L., Sys S.U., Gillebert T.C.
Diastolic failure: pathophysiology and therapeutic implications.
heart function. J Am Coll Cardiol 1993;22:318-25.
5. Soufer R., Wonlgelernter D., Vita N.A. et
al. Intact systolic left ventricular function in clinical congestive
heart failure. Am J Cardiol 1985;55:1032-36.
6. Vasan R.S., Benjamin E.J., Levy D. Prevalence,
clinical features and prognosis of diastolic heart failure: an
epidemiologic perspective. J Am Coll Cardiol 1995;26:1565-74.
7. European Study Group on Diastolic Heart Failure.
How to diagnose diastolic heart failure. Eur Heart J 1998;19:990-1003.
8. Ishikura F., Redfield M.M. Doppler echocardiography
assessment of diastolic function in congestive heart failure:
emphasis on clinical utility. Heart failure 1998;14:78-96.
9. ACC/AHA Task Force Report of the American
College of Cardiology/American Heart Association Task Force on
Practice Guidelines (Committee on evaluation and management of
heart failure). Guidelines for evaluation and management of heart
failure. Circulation 1995;92:2764-84.
10. Rhako P.S. Evaluation of left ventricular
filling in dilated cardiomyopathy using digitized M-mode echocardiograms.
Echocardiography 1991;8:163.
11. Bahler R.C. et al. The relation of heart
rate and shortening fraction to echocardiographic indexes of left
ventricular relaxation in normal subjects. J Am Coll Cardiol 1983;2:926.
12. Alam M., Hoglund C. Assessment by echocardiogram
of left ventricular diastolic function in healthy subjects using
the atrioventricular plane displacement. Am J Cardiol 1992;69:565.
13. Perez J.E., Waggoner A.D., Barzilai B. et
al. On-line assessment of left ventricular function by automatic
boundary detection and ultrasonic backscatter imaging. J Am Coll
Cardiol 1992;19:313.
14. Kitabatake A., Inoure M., Asao M. et al.
Transmitral blood flow reflecting diastolic behavior of the left
ventricular in health and disease. A study by pulsed Doppler technique.
Jpn Circ J 1982;46:92-102.
15. Little W.C., Downes T.R. Clinical evaluation
of left ventricular diastolic performance. Prog Cardiovasc Dis
1990;32:273-90.
16. Bonow R.O., Udelson J.E. Left ventricular
diastolic dysfunction as a cause of congestive heart failure.
Ann Intern Med 1992;117:502-10.
17. Brutsaert D.L., Sys S.U. Systolic and diastolic
heart function. J Cardiovasc Pharm 1996;28 (suppl 2):S1-S8.
18. Brutsaert D.L., Rademakers F.E., Sys S.U.
Triple control of relaxation: Implications in cardiac disease.
Circulation 1984;69:190-6.
19. Gilbert J.C., Glantz S.A. Determinants of
left ventricular filling and of the diastolic presse-volume relation.
Circ Res 1989;64:827-52.
20. Glantz S.A., Parmley W.W. Factors which
affect the diastolic presse-volume relation . Circ Res 1978;42
171.
21. Shabetai R. Progress in cardiac tamponade
and constrictive pericarditis, in P.N. Yu, J.F. Goodwin (eds):
Progress in Cardiology. Philadelphia, p.a., Lea and Febieer, 1986,
pp 87-98.
22. Little W.C., Badke F.R., O"Rourke R.A. Effect
of right ventricular pressure on the end-diastolic left ventricular
presse-volume relationship before and after chronic right ventricular
overload. Circ Res 1984;54:719-30.
23. Gaasch W.H., Bing O.H., Franklin A. et al.
The influence of ocute alterations in coronary blood on left ventricular
diastolic compliance and wall thickness. Eur J Cardiol 1978;7:147.
24. Gardin J.M., Dabestini A., Takenaka K. et
al. Effect of imaging view and sample volume location on evaluation
of mitral flow velocity by pulsed Doppler echocardiography. Am
J Cardiol 1986;57:1335-9.
25. Yamamoto K., Redfield M.M., Nishimura R.A..
Analysis of left ventricular diastolic function. Heart 1996;75(suppl
2):27-35.
26. Nishimura R.A., Abel M.D., Hatle L.K., Tajik
A.J. Assessment of diastolic function of the heart; background
and current applications of Doppler echocardiography. Part II.
Clinical studies. Mayo Clin Proc 1989;64:181-204.
27. Appleton Ch.P., Hatle L.K., Popp R.L. Relation
of transmitral flow velocity patterns to left ventricular diastolic
function: new insights from a combined hemodynamic and Doppler
echocardiographic study. J Am Coll Cardiol 1988;12:426-40.
42. Yamamoto K., Masuyama T., Tanouchi J. et
al. Importance of left ventricular minimal pressure as a determinant
of transmitral flow velocity patt erns to left ventricular diastolic
function: new insights from a combined hemodynamic and Doppler
echocardiographic study. J Am Coll Cardiol 1988;12:426-40.
28. Thomas J.D., Weyman A.E. Echocardiographic
Doppler evaluation of left ventricular diastolic function: Physics
and physiology. Circulation 1991;84:977-90.
29. Masuyama T., Popp R.L. Doppler evaluation
of left ventricular filling in congestive heart failure. Eur Heart
J 1997;18:1548-56.
30. Ishikura F., Redfield M.M. Doppler echocardiography
assessment of diastolic function in congestive heart failure:
emphasis on clinical utility. Heart failure 1998;14:78-96.
31. Miyatake K., Okamoto M., Kinoshita N. et
al. Augmentation of atrial contribution to left ventricular inflow
with aging as assessed by intracardiac Doppler flowmetry. Am J
Cardiol 1984;53:586-9.
32. Benjamin E.J., Levy D., Anderson K.M. et
al. Determinants of Doppler indexes of left ventricular diastolic
function in normal subjects (the Framingham Heart Study). Am J
Cardiol 1992;70:508-15.
33. Jensen J.L., Williams F.E., Beildy B.J.
et al. Feasibility of obtaining pulmonary venous flow velocity
in cardiac patients using transthoracic pulsed wave Doppler technique.
J Am Soc Echocardigr 1997;10:60-66.
34. Klein A.L., Tajik A.J. Doppler assessment
of pulmonary venous flow in healthy subjects and in patients with
heart disease. J Am Soc Echocardigr 1991;4:379-92.
35. Appleton C. Doppler assessment of left ventricular
diastolic function: the refinements continue. J Am Coll Cardiol
1993;21:1697-700.
36. Rossvoll O., Hatle L.H. Pulmonary venous
flow velocity recorded by transthoracic Doppler ultrasound: relation
to left ventricular diastolic pressures. J Am Coll Cardiol 1993;21:1687-96.
37. Nagano R., Masuyama T., Lee J.M. et al.
Transthoracic Doppler assessment of pattern of left ventricular
dysfunction in hypertensive heart disease: Combined analysis of
mitral and pulmonary venous flow velocity patterns. J Am Soc Echocardigr
1994;7:493-505.
38. Dumesnil J.G., Gaudreault G., Honos G.N.
et al. Use of Valsalva maneuver to unmask left ventricular diastolic
function abnormalities by Doppler echocardiography in patients
with coronary artery disease or systemic hypertension. Am J Cardiol
1991;68:515-19.
39. Yamamoto K., Masuyama T., Tanouchi J. et
al. Intraventricular dispersion of early diastolic filling: a
new marker of left ventricular diastolic dysfunction. Am Heart
J 1995;129:291-9.
40. Brun P., Tribouilloy C., Duval A.M. et al.
Left ventricular flow propogation during early filling is related
to wall relaxation. A color M-mode Doppler analysis. J Am Coll
Cardiol 1992;20:420-32.
41. Stuggard M., Risoe C., Ihlen H., Smiseth
O.A. Intracavitary filling pattern in the failing left ventricle
assessed by color M-mode Doppler chocardiography. J Am Coll Cardiol
1994;24:663-70.
42. Yamamoto K., Masuyama T., Tanouchi J. et
al. Importance of left ventricular minimal pressure as a determinant
of transmitral flow velocity pattern in the presence of left ventricular
systolic dysfunction. J Am Coll Cardiol 1993;21:662-72.
/ 16.01.2018
Диастолическая функция левого желудочка норма. Понятие о систолической и диастолической недостаточности
В современной терминологии - систолическая сердечная недостаточность. Однако в конце 1970-х - 80-х годов стало ясно, что значительная часть больных с клинической картиной сердечной недостаточности имеют нормальную сократительную функцию сердца, нормальные значения фракции выброса левого желудочка. Такая клиническая картина в современной терминологии описана как диастолическая сердечная недостаточность.
Изучение диастолы и, по сути, заболеваний, связанных с ее изменениями, начато еще в 1877 г., когда Francois-Franck на основании опытов заключил, что максимальное заполнение левого желудочка кровью происходит в ранней диастоле. В 1906 г. Hendorson описал три фазы диастолы, а в 1921 г. Wiggers и Katz выяснили, что вклад левого предсердия в заполнение кровью левого желудочка может возрастать у людей с измененными свойствами ЛЖ. В 1927 г. Meek в эксперименте установил, что фаза активной релаксации миокарда в диастолу влияет на сократимость миокарда. В 1949 г. Wiggers ввел термин «присущая эластичность» для описания поведения миокарда ЛЖ в период диастолы, т.е. предпринял попытку описать основное состояние миокарда в диастолу - расслабление.
В 1975 г. W.H. Gaasch в серии экспериментальных и клинических работ определил различия в диастоле у здоровых людей и больных сердечно-сосудистыми заболеваниями, используя изменение давления в полости ЛЖ и изменение его объема. В частности, установлено, что объем крови при пассивном заполнении ЛЖ уменьшен у больных с сердечно-сосудистыми заболеваниями. В 1983-1984 гг. Н.Н. Echeverria, А.Н. Dougherty, R. Souter ввели в клиническую практику термин «диастолическая сердечная недостаточность».
Диастолическая сердечная недостаточность (ДСН) - клинический синдром с симптомами и признаками сердечной недостаточности, нормальной ФВ ЛЖ и нарушением его диастолической функции.
Клинически диастолическая сердечная недостаточность проявляется как незначительным ограничением физической активности (I ФК по классификации NYHA ассоциации по изучению заболеваний сердца), так и наличием симптомов в покое (IV ФК).
Нормальная диастолическая функция ЛЖ - способность его «принимать» объем крови, необходимый для поддержания адекватного сердечного выброса , без повышения среднего легочного венозного давления (>12 мм рт.ст.). Диастолическая дисфункция ЛЖ возникает, если поступление в ЛЖ должного объема крови возможно лишь за счет повышения давления его наполнения или если он не способен во время нагрузки увеличивать наполнение и тем самым обеспечить адекватное увеличение сердечного выброса. Любое повышение давления наполнения ЛЖ всегда свидетельствует о диастолической дисфункции. Практически у всех больных с систолической дисфункцией ЛЖ сердца существуют нарушения диастолической его функции.
Диастола ограничена промежутком времени от закрытия аортального клапана до закрытия митрального клапана . Два ключевых механизма происходят в диастолу - расслабление ЛЖ и его наполнение. Расслабление ЛЖ начинается уже во вторую половину систолы (в период замедленного изгнания крови), достигает максимума во время фазы изоволюметрического расслабления и оканчивается уже во время наполнения ЛЖ, которое состоит из фаз быстрого наполнения, замедленного наполнения (диастазиса) и систолы предсердий.
Диастолическая функция ЛЖ зависит от способности миокарда расслабиться, которая зависит от функционирования саркоплазматического ретикулума кардиомиоцитов.
Диастолическая функция ЛЖ зависит и от механических свойств миокарда - эластичность (изменение длины мышечных волокон в зависимости от приложенной к ним силы), податливость (изменение объема желудочка при заданном изменении давления) и жесткость (характеристика, обратная податливости). Пассивные характеристики сердца отражают способность ЛЖ к растяжению по мере поступления в него крови.
В молодом возрасте наполнение ЛЖ обусловлено высоким градиентом давления в начале диастолы, который формируют высокая скорость расслабления и эластические свойства миокарда. В этой ситуации ЛЖ в основном заполняется кровью в первой половине диастолы.
Старение, АГ, ИБС приводят к значимому замедлению процессов расслабления. В такой ситуации заполнение ЛЖ кровью происходит в основном не в первой половине диастолы, а в систолу левого предсердия.
На диастолическую функцию миокарда существенное влияние оказывают состояние (размер, объем) левого предсердия, скорость трансмитрального кровотока и число сердечных сокращений
Изменение объема поступающей в левое предсердие крови меняет его сократительную способность в полном соответствии с законом Старлинга. Возросшая сила сокращения левого предсердия порождает ударную струю, которая изменяет скорость заполнения ЛЖ и смещает во времени последующие фазы, повышая жесткость миокарда Эти изменения очевидны при АВ-блокадах, большой ЧСС и перегрузке объемом крови левого предсердия.
Симптомы и признаки диастолическая дисфункция левого желудка
Больные с диастолической сердечной недостаточности предъявляют те же жалобы, что и больные с сердечной недостаточностью, - чувство нехватки воздуха, утомляемость, сердцебиение.
У больных с диастолической сердечной недостаточностью чаще встречают АГ и реже постинфарктный кардиосклероз. Такие больные обычно старше больных с систолической сердечной недостаточностью, и часто имеют избыточную массу тела. Для больных с диастолической формой сердечности недостаточности характерна мерцательная аритмия (среди пожилых пациентов - до 75%).
У больных с диастолической сердечной недостаточностью реже встречаются признаки венозного застоя и связанные с ним симптомы (отеки, хрипы в легких, набухание шейных вен, удушье) по сравнению с больными с классической, систолической формой заболевания.
При аускультации больных с диастолической сердечной недостаточностью часто можно выслушать 4 тона сердца. Хотя обнаружение III тона сердца более характерно для больных с систолической сердечной недостаточностью. При выраженной диастолической дисфункции, особенно при рестриктивном типе наполнения ЛЖ, этот признак обнаруживают очень часто.
Самое крупное клинико-эпидемиологическое исследование клинической картины недостаточности кровообращения - исследование, выполненное в РФ (ЭПОХА-О-ХСН) в 2001-2002 гг.
Полученными данными отмечена тенденция к увеличению распространенности диастолической сердечной недостаточности за последние годы. Нормальную систолическую функцию ЛЖ регистрируют у 35-40% больных с сердечной недостаточностью. Распространенность диастолической сердечной недостаточности зависит от возраста. У больных в возрасте не старше 50 лет диастолическую форму диагностируют у 15% больных, в возрасте старше 70 лет - уже у 50% больных.
Частота встречаемости сердечной недостаточности с нормальной систолической функцией ЛЖ зависит от тяжести обследуемых больных и критериев оценки систолической функции. Так, среди больных, госпитализированных с декомпенсацией сердечной деятельности, нормальную ФВ ЛЖ регистрируют у 20-30% больных, а при терминальной сердечной недостаточности - у 5-10% больных. В то же время в амбулаторной практике распространенность сердечной недостаточности с нормальной систолической функцией ЛЖ, диагностированной с использованием «мягких» критериев (например, на основании превышения фракции выброса на 40%), достигает 80%. Таким образом, по мере повышения степени тяжести сердечной недостаточности вклад изолированной диастолической дисфункции как основной причины сердечной недостаточности снижается.
Прогноз диастолической сердечной недостаточности
- Частота повторных госпитализаций больных с ДСН и у больных с систолической недостаточностью не различаются - примерно 50% в год.
- Смертность у больных с ДСН - 5-8% в год (при систолической недостаточности кровообращения - 15% в год). За последние годы не отмечено снижение уровня смертности при ДСН.
- Смертность при диастолической сердечной недостаточности зависит от причины СН, при неишемическом ее генезе - 3% в год.
Диагностика диастолической сердечной недостаточности
Диагноз диастолической дисфункции верифицирован, если у больного имеются 3 критерия.
- Симптомы или признаки сердечной недостаточности.
- Нормальная или незначительно сниженная сократительная функция ЛЖ (ФВ ЛЖ >45% и индекс его конечно-диастолического размера
- Признаки нарушения расслабления или наполнения ЛЖ, повышенной его жесткости, полученные при инструментальных методах исследования.
Основа диагностики диастолической сердечной недостаточности - ЭхоКГ.
Диастолический подъем основания левого желудочка. При диастолической дисфункции максимальная скорость раннего диастолического подъема основания ЛЖ (E m) ниже 8 см/с. Кроме того, отношение максимальных скоростей волны трансмитрального кровотока Е и Е >15 свидетельствует о повышенном конечно-диастолическом давлении в ЛЖ (>12 мм рт.ст.), Е/Е m
Общепринятый биохимический маркер диастолической сердечной недостаточности - предшественник мозгового натрийуретического пептида (NT-pro-BNP). Для диастолической сердечной недостаточности характерно повышение уровня этого пептида.
Лечение диастолической сердечной недостаточности
Лечение ишемии миокарда. ИБС - один из главных факторов, располагающих к диастолическим нарушениям. Те или иные расстройства диастолы выявляются более чем у 90% больных с ИБС. Улучшение диастолической функции в условиях ИБС возможно при использовании лекарственных средств (β-ацреноблокаторы, антагонисты кальция) и мер по реваскуляризации миокарда.
Лечение артериальной гипертензии. У больных с АГ диастолическая дисфункция ЛЖ - одно из ранних и распространенных проявлений дисфункции миокарда, особенно на стадии гипертрофии миокарда. Нормализация АД - один из простых и в то же время эффективных способов улучшения диастолического наполнения ЛЖ.
Снижение давления наполнения ЛЖ (уменьшение его преднагрузки). Важнейший принцип лечения этого состояния - снижение преднагрузки ЛЖ (использование диуретиков). Избыточное снижение преднагрузки резко уменьшает объем наполнения ЛЖ и снижает сердечный выброс. В этих случаях оправданна тактика медленного снижения преднагрузки на ЛЖ. Прием мочегонных средств сопровождается избыточной активацией ренин-ангиотензиновой системы, поэтому целесообразно их сочетание с блокаторами ренин-ангиотензиновой системы (иАПФ, блокаторы ангиотензиновых рецепторов, антагонисты альдостерона).
Поддержание и/или восстановление синусового ритма, сохранение сократительной функции левого предсердия. Сократительная функция левого предсердия играет важнейшую роль в обеспечении нормальной переносимости физических нагрузок в условиях диастолической сердечной недостаточности, прогрессирование которой резко повышает риск мерцательной аритмии. При мерцательной аритмии врач выбирает тактику «контроль ритма» или «контроль частоты». Тщательное выполнение требований выбранной тактики предотвращает прогрессирование диастолической сердечной недостаточности.
Больные с диастолической сердечной недостаточностью должны иметь целевые уровни ЧСС: при ИБС - 55-60 в мин. При ХСН снижение на 16% исходной ЧСС (80-84 в мин) сопровождается снижением риска смерти. Для снижения ЧСС используют β-адреноблокаторы, фенилалкиламины и блокаторы If каналов.

Вероятность того, что у людей с тем или иным «сердечным» диагнозом выявят признаки диастолической дисфункции левого желудочка, чрезвычайно велика, к примеру, подобным нарушением страдают от 50 до 90 процентов больных артериальной гипертензией.
На первый взгляд может показаться, что сбои в работе отдельной части миокарда, тем более, если они не имеют ярко выраженной симптоматики, не несут опасности для здоровья. На самом деле, при отсутствии грамотного лечения, диастолическая дисфункция левого желудочка может вызвать серьезные перепады артериального давления, спровоцировать аритмию и прочие неприятные последствия. В связи с этим врачи настоятельно рекомендуют внимательно относиться к состоянию главной мышцы организма и при любом намеке на патологию обращаться к специалисту. Особенно актуальным этот совет является для тех, у кого есть врожденная или приобретенная патология сердца.
Интересно! Среди ученых-медиков нет единого мнения по поводу того, возникает ли нарушение диастолической функции левого желудочка у всех сердечников, однако точно установлено, что наибольшему риску подвержены пожилые люди и страдающие от ХСН. Также известно, что по мере ухудшения состояния данная патология прогрессирует.
Отличительные особенности нарушения
В неспециализированной литературе диастолическое нарушение левого желудочка часто используют как синоним диастолической сердечной недостаточности, хотя эти понятия нельзя назвать идентичными. Дело в том, что при наличии ДСН всегда фиксируется снижение эластичности левой части миокарда, однако зачастую подобная проблема является только предвестником систолического сбоя.
Далеко не всегда, человеку, у которого выявили снижение диастолической функции левого желудочка, в конечном счете, ставят диагноз, поскольку для этого необходимо также наличие других характерных признаков, а также небольшое снижение показателей фракции выброса. Решение о постановке диагноза принимается доктором после тщательного исследования работоспособности всех частей миокарда, а также на основе результатов диагностических процедур.
Что вызывает снижение диастолической функции?
Причин, почему диастолическая функция нарушена, может быть достаточно много, причем у каждого человека патология проявляется по-разному и может быть спровоцирована как внутренними нарушениями, так и внешними факторами. Среди наиболее часто встречающихся причин:
- значительное сужение просвета аорты вследствие сращивания створок клапана ();
- ишемическая болезнь сердца;
- регулярное повышение показателей артериального давления;
- избыточный вес;
- пожилой возраст.
Впрочем, диастолическая дисфункция левого желудочка возникает и в ряде других случаев, например, при наличии серьезного поражения миокарда (кардиомиопатии, болезни эндокарда и т.д.), а также системных сбоях, вызванных амилоидозом, гемохроматозом, гиперэозинофильным синдромом и т.д. Редко, однако, возможно развитие патологии при выпотном констриктивном перикардите и при болезни накопления гликогена.
Возможные симптомы и проявление дисфункции
Внутренние и внешние проявления диастолической дисфункции зависят от многих факторов, в частности, от состояния сердечной мышцы, а точнее – эластичности стенок и успешности релаксации главной мышцы организма.

Если диастолическая функция левого желудочка по тем или иным причинам нарушена, то происходит возрастание давления наполнения для поддержания показателей вырабатываемого объема крови, который необходим для нормального функционирования органов. В результате сбоя, как правило, возникает одышка, которая свидетельствует о наличии застоя в легких.
Важно! Если не избавиться от чрезмерного давления к легочному руслу, то есть опасность, что дисфункция впоследствии перерастет в правостороннюю сердечную недостаточность.
Если патология находится в умеренной фазе, то симптомы проявляются периодически, а сердце постепенно возвращается в норму, однако в тяжелых случаях ригидность достигает такого большого значения, что предсердия не могут компенсировать необходимый объем. Исходя из клинической картины и степени повреждений, выделяют такие типы диастолической дисфункции левого желудочка:
- I тип – в основном является результатом возрастных изменений структуры желудочков, проявляясь в снижении фракции перекачивания крови и общему уменьшению объема крови с одновременным увеличением систолического объема. Наиболее серьезным осложнением является развитие венозного застоя, хотя также опасность несет вторичная легочная гипертензия;
- II тип (рестриктивный) – сопровождается серьезным увеличением ригидности, вызывающего существенный градиент давления между камерами на начальном этапе диастолы, что сопровождается сменой характера трансмитрального кровотока.
Комплексный подход – залог эффективной терапии

От причины и правильности диагностики напрямую зависит, как быстро может быть вылечена диастолическая дисфункция левого желудочка. Лечение данной патологии направлено в первую очередь на нейтрализацию провоцирующих факторов, а также избавление от основного заболевания сердечно-сосудистой системы, например, ИБС или гипертензии.
Иногда с целью восстановления миокарда проводят хирургическую операцию по извлечению поврежденного перикарда, хотя чаще всего терапия ограничивается приемом медикаментов, а именно:
- ингибиторов АПФ, БРА;
- бета-блокаторов;
- диуретиков;
- блокаторов кальциевых каналов и т.д.
Помимо этого, для поддержания нормального состояния «внутреннего двигателя» больным с нарушением диастолической функции назначают диету с ограниченным количеством натрия, рекомендуют физические управления (особенно, если имеется лишний вес), а также устанавливаются ограничения по количеству употребляемой жидкости.
Вконтакте
Всем нам знакома фраза: «…а вместо сердца пламенный мотор». Также довольно точно сердце сравнивают с насосом, а в кардиологии есть такое понятие как «насосная функция» миокарда. Понятно, что систола левого желудочка выбрасывает объем крови в аорту. А диастола – это период отдыха (расслабления) желудочков. Именно в период диастолы они заполняются кровью. Роль этого периода цикла сердечного сокращения весьма значительна: какова диастола, такова будет и последующая систола. Какие признаки диастолической дисфункции существуют у левого желудочка?
О систоле желудочков известно гораздо больше, чем о диастоле. Несмотря на более чем 50-летнее изучение диастолы продвинуться вперед оказалось сложно даже с применением современных способов исследования и визуализации миокарда. Прежде всего, при формировании хронической сердечной недостаточности важна систолическая функция, которую и исследовали.
Кроме того, ранняя диагностика диастолической дисфункции затруднена еще и тем, что она протекает полностью бессимптомно. На более поздних стадиях к ней присоединяются систолические нарушения, которые и заставляют пациента обращаться к врачу. Тем не менее, в период развития симптоматики именно диастолическая дисфункция левого желудочка обуславливает развитие хронической сердечной недостаточности у 35 – 40% всех пациентов. Сложность также в том, что, несмотря на очевидную простоту, среди кардиологов, физиологов и патофизиологов нет определения того, что такое диастола. «Бытовой» термин о том, что это состояние расслабления желудочков их не устраивает. Как минимум, диастола включает в себя:
- мышечное расслабление;
- пассивное всасывание;
- наполнение кровью;
- систола предсердий – активный процесс.
Уже появились серьезные поводы к тому, чтобы в экспериментальной физиологии сердечных сокращений ввести новую научную дисциплину – диастологию. Это говорит о важности диастолы. Диастолическая дисфункция – это состояние, при котором мышечные волокна миокарда не могут расслабиться, когда это нужно. Это приводит к недостаточному накоплению крови в полости левого желудочка и, соответственно, к недостаточному сердечному выбросу в аорту во время систолы. Нужно понимать, что диастолическая дисфункция поражает сразу оба желудочка. Не бывает так, что правый желудочек работает идеально, а левый – «хромает». Скоро нарушение кровенаполнения желудочков вызывает перегрузку предсердий.
Классификация
Существует несколько типов развития этого нарушения у пациентов:

Все вышеописанные варианты ведут к нарушению сократительной способности миокарда, то есть сказываются на кровообращении. Причиной развития дисфункции может быть фиброз сердечной мышцы, ее тотальная или очаговая гипертрофия, ишемия, в том числе с развитием постинфарктного кардиосклероза. В результате этих процессов повышается количество ионов кальция в миокардиоцитах и снижаются резервные возможности сердечной мышцы.
Одним из средств диагностики этого отклонения от нормы является УЗИ сердца с оценкой ТМДП (трансмитрального диастолического потока). Этот поток является количественным показателем крови, попадающей в левый желудочек через митральный клапан, который соединяет левое предсердие с левым желудочком. В середине восьмидесятых годов прошлого века выяснилось, что оценка спектра ТМДП довольно точно совпадает со степенью тяжести хронической сердечной недостаточности, что позволяет выставить различные варианты прогноза течения заболевания.
Вообще, диастолическая дисфункция и ее показатели гораздо лучше связаны с оценкой степени хронической сердечной недостаточности, чем нарушения систолического кровотока. Именно диастолические расстройства и определяют всю тяжесть сердечных застойных явлений, таких, например, как отеки.
Лечение такого нарушения обязательно является комплексным. Обязательно нужна профилактика аритмии – восстановление ритма при мерцании предсердий. Кроме этого, рекомендуются препараты, которые замедляют проведение импульсов от предсердий к желудочкам. Это позволяет лучше расслабиться предсердиям. Также показан прием нитратов, диуретиков (с целью ликвидировать отеки и застой в легких), а также ингибиторов АПФ, которые расслабляют миокард. Если есть сохранность систолической функции, прием сердечных гликозидов не разрешается. В любом случае терапия диастолической дисфункции неотделима от лечения основного заболевания (аритмий, ИБС, другой патологии сердечнососудистой системы).
Определение диастолической дисфункции (или типа диастолического наполнения) основано на нескольких признаках. При большинстве (если не при всех) заболеваниях сердца сначала нарушается процесс расслабления миокарда. При прогрессировании болезни и повышении давления в ЛП от легкого до умеренного скорость ТМП напоминает нормальную (псевдонормализация). При дальнейшем снижении податливости миокарда ЛЖ и увеличении давления в ЛП диастолическое наполнение становится рестриктивным.
У большинства больных с рестриктивным типом диастолической дисфункции присутствуют клиническая симптоматика и плохой прогноз, за исключением тех случаев, когда рестриктивный тип может претерпеть обратное развитие после лечения. Рестриктивный тип может быть необратимым и представлять конечную стадию диастолической си. Таким образом, на основе типа диастолического наполнения можно выделить следующие степени диастолической дисфункции:
Степень 1 (легкая дисфункция) нарушенная релаксация с нормальным давлением наполнения;
степень 2 (умеренная дисфункции) - псевдонормальная картина ТМП;
степень 3 (тяжелая обратимая дисфункции) - обратимая рестрикция (высокое давление наполнения);
степень 4 (тяжелая необратимая дисфункция) - необратимая рестрикция (высокое давление наполнения).
Для диастолической дисфункции степени 1 характерно нормальное давление наполнении, несмотря на имеющееся нарушение расслабления миокарда. Однако у больных С выраженным нарушением релаксации, например при ГКМП, давление может быть повышенным (Е/А 2 10 меск). Это состояние называют диастолической дисфункцией степени 1а (гемодинамически она напоминает диастолическую дисфункцию степени 2).
У молодых пациентов пластическое притяжение ЛЖ в норме сильно выражено, что связано с нормальной релаксацией, поэтому основное наполнение ЛЖ происходит в раннюю диастолу. В результате обычно Е/А > 1,5, DT = 160-240 мсек (в области перегородки), Еа > 10 см/сек, E/Еа 50 см/сек. Такое сильное расслабление у здоровых лиц проявляется активным движением митрального кольца от верхушки в раннюю диастолу при парастернальной позиции но длинной оси и апикальной четырехкамерной позиции.
При нормальном миокардиальным расслаблении картина скорости продольного движения митрального кольца во время диастолы является зеркальным отражением нормального трансмитрального кровотока: скорость кровотока в раннюю диастолу (Еа) выше, чем скорость кровотока в позднюю диастолу (Аа). Скорость латерального отдела кольца МК всегда выше (в норме > 15 см/сек), чем септального. Еа у здоровых лиц увеличивается при нагрузке, однако соотношение Е/Еа остается таким же, как в покое (обычно
С возрастом происходит постепенное снижение скорости расслабления миокарда, а также эластического притяжения, что приводит к более медленному снижению давления в ЛЖ. Наполнение его становится более медленным, что способствует развитию картины, сходной с диастолической дисфункцией степени 1. К = 65 годам скорость пика Е достигает скорости пика А, и у лиц старше 70 лет соотношение Е/А обычно
Реверсия соотношения Еа/Аа наступает на 10-15 лет раньше, чем Е/А. Скорость кровотока н легочных венах с возрастом также меняется: скорость ортоградного диастолического кровотока снижается по мере наполнения ЛЖ во время сокращения предсердий, и скорость ортоградного систолического кровотока становится более значительной.
Изучение диастоличсской функции у 1012 лиц без ССЗ в анамнезе при двухмерной ЭхоКГ показали, что все параметры диастоличсской функции ассоциированы с возрастом.
Сердечная недостаточность - это неспособность сердца забирать кровь из емкостных сосудов, вызывать легочное кровообращение и выбрасывать кровь в аорту в соответствии с потребностями организма при нормальном общем венозном возврате. Иными словами, сердечная недостаточность - это падение производительности сердца как насоса системного кровообращения при нормальных объеме циркулирующей крови и тонусе емкостных сосудов, то есть при оптимальных величинах и состоянии детерминант общего венозного возврата.Причина сердечной недостаточности:
Наиболее частая причина сердечной недостаточности - это систолическая дисфункция левого желудочка. Систолическая дисфункция левого желудочка - это снижение способности левого желудочка выбрасывать кровь из своей полости в аорту. Систолическую дисфункцию вызывает падение сократимости левого желудочка, снижающее его ударный объем. Систолическая дисфункция обуславливает недостаточность минутного объема кровообращения (МОК), то есть несоответствие относительно низкой величины МОК потребностям всего организма.Систолическая дисфункция вызывает компенсаторную дилатацию левого желудочка.
В результате дилатации растет конечный систолический объем левого желудочка. Рост конечного систолического объема демпфирует рост конечного систолического давления левого желудочка, обусловленный падением его фракции изгнания и ударного объема.
Таким образом, дилатация предотвращает застой крови в легких, обусловленный систолической дисфункцией. Когда данная компенсаторная реакция становится несостоятельной, возникает вторичная легочная венозная гипертензия. Легочная артериальная гипертензия (следствие легочной венозной гипертензии) повышает постнагрузку правого желудочка. Его ударный объем падает. Падение ударного объема повышает давление крови в правом желудочке (конечное систолическое, конечное диастолическое). Рост конечного диастолического давления правых желудочка и предсердия вызывает общую венозную гиперемию.
Диастолическая дисфункция левого желудочка - это падение его способности перекачивать кровь из системы легочной артерии в свою полость, то есть активно обеспечивать свое диастолическое наполнение. Диастолическая дисфункция проявляется ростом отношения конечного диастолического давления левого желудочка к его конечному диастолическому объему.
Патогенез диастолической дисфункции во многом составляется падением податливости стенок левого желудочка.
Выделяют три главных этапа диастолического наполнения левого желудочка:
1. Релаксация.
2. Пассивное заполнение.
3. Заполнение посредством сокращения предсердий.
В основе релаксации лежит активное выведение кальция из нитей актина-миозина, которое расслабляет сокращенные саркомеры миокарда и увеличивает их длину. В результате длина саркомеров возвращается на конечный диастолический уровень. При ишемии гипоэргоз клеток сердца угнетает активное выведение кальция, и релаксация становится недостаточной. Снижение релаксации уменьшает диастолическое наполнение. Снижение диастолического наполнения вызывает легочные вторичные венозную и артериальную гипертензии и соответствующие симптомы (одышку, кашель и пароксизмальное ночное диспноэ).
После релаксации происходит пассивное наполнение полости левого желудочка кровью, которое происходит под действием градиента давлений между полостями левого предсердия и левого желудочка.
Детерминантой объема крови, поступающей при пассивном наполнении в желудочек, является податливость его стенок. Связанный с ишемией гипоэргоз угнетает выведение кальция из нитей актина-миозина и снижает податливость. Снижение податливости уменьшает пассивное наполнение.
В физиологических условиях 15-20% конечного диастолического объема левого желудочка поступает в его полость посредством активного сокращения стенок левого предсердия. При ригидности стенок левого желудочка посредством сокращения стенок левого предсердия в левый желудочек поступают 45-50% конечного диастолического объема. У больных с ишемией и патологической ригидностью стенок левого желудочка мерцательная аритмия резко повышает вероятность кардиогенного отека легких.
Дело в том что мерцательная аритмия нарушает согласованность сокращений саркомеров миокарда левого предсердия. В результате снижается диастолическое наполнение посредством сокращения левого предсердия. При этом, несмотря на компенсаторную дилатацию левого предсердия, в нем растет среднее давление. Рост среднего давления в левом предсердии вызывает легочную венозную гипертензию и кардиогенный отек легких.
Причины дисфункции левого желудочка:
К причинам диастолической дисфункции левого желудочка относят:1) системные инфильтративные болезни на уровне сердца (амилоидоз и др.);
2) гипертоническую болезнь с патологической гипертрофией левого желудочка;
3) гипертрофическую кардиомиопатию.
Следует заметить, что у 30-40% больных с сердечной недостаточностью нет систолической дисфункции левого желудочка.
Чаще всего острая сердечная недостаточность - это быстро развившаяся систолическая или диастолическая дисфункция левого желудочка. При острой систолической дисфункции ударный объем левого желудочка снижается в такой степени, что падение МОК обуславливает артериальную гипокапнию и циркуляторную гипоксию. При острой диастолической дисфункции вторичная легочная венозная гипертензия обуславливает отек легких.
Наиболее частая причина сердечной недостаточности - это ишемическая болезнь сердца и ее последствия. В результате обширного инфаркта происходит ремоделирование желудочка, то есть эксцентрическая и концентрическая гипертрофия сегментов сердца, не вовлеченных в зону инфаркта при истончении и дилатации сегментов в зоне инфаркта. Факторами риска ремоделирования являются неэффективная реваскуляризация в остром периоде, обширный инфаркт , инфаркт передней локализации, а также хроническая артериальная гипертензия. Ремоделирование дискоординирует сокращение и расслабление сегментов, что служит причиной как систолической, так и диастолической дисфункции.
Часть кардиомиоцитов в зоне инфаркта сохраняют жизнеспособность посредством гибернации, то есть перестают сокращаться и всю доступную свободную энергию расходуют исключительно на сохранение жизнеспособности. Реваскуляризация восстанавливает сокращения данных клеток рабочего миокарда. Если сократительная функция не восстанавливается реваскуляризацией, но клетки сохраняют жизнеспособность, то говорят о станинге. И станнинг, и гибернация могут быть звеньями патогенеза систолической и диастолической дисфункции.
Патогенез застойной сердечной недостаточности:
Сердечная недостаточность - это патологическое состояние аномальных изменений миокарда, скелетных мышц, расстройств функций почек, избыточной активации симпатического отдела автономной нервной системы и других сложных расстройств нейрогуморальной регуляции. Стимулами для системных патологических реакций, вызывающих звенья патогенеза сердечной недостаточности и свойственные данному патологическому состоянию расстройства нейрогуморальной регуляции, являются систолическая дисфункция левого желудочка и падение минутного объема кровообращения. Вследствие низкого ударного объема, а также снижения скорости выброса крови в аорту падает наполнение кровью артериального русла. В результате снижается уровень возбуждения барорецепторов артериальной стенки, что растормаживает симпатические кардиостимулирующие и вазоконстрикторные нейроны сосудодвигательного центра продолговатого мозга.В частности, патологическое состояние сердечной недостаточности вызывается и составляется активацией ренин-ангиотензин-альдостеронового механизма. Вследствие активации механизма в плазме крови растут активность ренина, а также концентрация ангиотензина-II. Под действием ангиотензина-II усиливается высвобождение норадреналина симпатическими нервными окончаниями, ослабляются вагальные влияния, а также интенсифицируется секреция альдостерона. В результате повышается общее периферическое сосудистое сопротивление, в организме задерживается натрий, возрастает объем внеклеточной жидкости, появляются отеки, а также увеличивается выделение калия вместе с мочой.
Все это повышает как преднагрузку сердца, так и его постнагрузку. У больных с ишемической болезнью сердца, вызывающей сердечную недостаточность, увеличение преднагрузки и постнагрузки повышает потребность сердца в кислороде, вызывая ишемию миокарда, что обуславливает прогрессирование ишемической дилатационной кардиомиопатии.
Кроме того, при сердечной недостаточности ангиотензин-II угнетает эндотелий-зависимую релаксацию венечных артерий и действует как фактор клеточного роста кардиомиоцитов, вызывающий патологическую гипертрофию левого желудочка.
Усиленная адренергическая стимуляция на периферии по мере возникновения и прогрессирования сердечной недостаточности раньше всего происходит на уровне сердца. По мере прогрессирования сердечной недостаточности последствия усиленной адренергической стимуляции начинают испытывать клетки произвольных мышц и почечная паренхима. Усиление адренергической стимуляции, повышающей уровень возбуждения 3-адренорецепторов почечной паренхимы - это один из факторов активации ренин-ангиотензин-альдостеронового механизма у больных с сердечной недостаточностью.
Избыточная адренергическая стимуляция миокарда индуцирует апоптоз мио-Цитов, служит одной из причин патологической гипертрофии левого желудочка, вызывая точечный некоронарогенный миокардиосклероз. При хронической сердечной недостаточности сердце реагирует на длительно сохраняющуюся высокую действующую концентрацию эндогенных катехоламинов в циркулирующей крови снижением чувствительности и числа своих B-адренорецепторов.
При этом патогенез сердечной недостаточности характеризуется угнетением функции барорецепторов. Угнетение функции барорецепторов ослабляет парасимпатические влияния на синоатриальный водитель ритма, что обуславливает патологически низкую вариабельность сердечного ритма.